Thành phần
Mỗi viên nang cứng chứa 200mg celecoxib.
Tá dược: Viên nang chứa lactose monohyđrat, natri lauryl sulfat, povidon K30, natri croscarmellose, magnesi stearat. Vỏ nang chứa gelatin, nước tinh khiết, natri lauryl sulfat, silic dioxid keo, titan dioxid; mực in chứa sắt oxid E172, shellac.
Công dụng (Chỉ định)
Điều trị triệu chứng của thoái hóa khớp (Osteoarthritis, OA) và viêm khớp dạng thấp (Rheumatois arthritis, RA).
Giảm nhẹ các dấu hiệu và triệu chứng của viêm cột sống dính khớp (Ankylosing spondylitis, AS).
Kiểm soát đau cấp tính
Điều trị thống kinh nguyên phát.
Cách dùng - Liều dùng
Viên nang Celecoxib, với liều dùng đến 200mg, 2 lần/ngày có thể dùng cùng thức ăn hoặc không.
Các nguy cơ trên tim mạch của celecoxib có thể tăng theo liều và thời gian dùng thuốc, nên dùng liều thấp nhất trong thời gian ngắn nhất có thể.
Người lớn
Điều trị triệu chứng trong thoái hóa khớp (OA): liều khuyến nghị của celecoxib là 200mg dùng liều đơn hoặc 100mg, 2 lần mỗi ngày.
Điều trị triệu chứng trong viêm khớp dạng thấp (RA): liều khuyến nghị của celecoxib là 100mg hoặc 200mg 2 lần mỗi ngày.
Viêm cột sống dính khớp (AS): liều khuyến nghị của celecoxib là 200mg dùng liều đơn hoặc 100mg dùng 2 lần mỗi ngày. Một số bệnh nhân có thể đạt hiệu quả điều trị tốt hơn nếu dùng tổng liều mỗi ngày 400mg.
Kiểm soát đau cấp tính: liều khuyến nghị khởi đầu của celecoxib là 400mg, dùng tiếp theo liều 200mg nếu cần trong ngày đầu tiên. Trong các ngày tiếp theo, liều khuyến nghị là 200mg 2 lần mỗi ngày khi cần.
Điều trị đau bụng kinh nguyên phát: liều khuyến nghị khởi đầu của celecoxib là 400mg, tiếp theo với liều bổ sung 200mg trong ngày đầu tiên nếu cần. Trong các ngày tiếp theo, liều khuyến nghị là 200mg 2 lần mỗi ngày khi cần.
Những người chuyển hóa kém qua CYP2C9: Những bệnh nhân đã biết hoặc nghi ngờ chuyển hóa kém qua CYP2C9 dựa trên tiền sử/kinh nghiệm với các cơ chất của CYP2C9 khác cần thận trọng khi dùng celecoxib. Bắt đầu điều trị với liều bằng ½ liều khuyến nghị thấp nhất (xem phần Tương tác với các thuốc khác và các dạng tương tác khác và Chuyển hóa).
Người cao tuổi
Nhìn chung không phải điều chỉnh liều. Tuy nhiên, với các bệnh nhân cao tuổi có cân nặng dưới 50kg, nên bắt đầu điều trị với liều khuyến nghị thấp nhất.
Cách dùng
Với bệnh nhân khó nuốt viên nang, có thể cho lượng thuốc trong viên vào sinh tố táo, cháo, sữa chua hoặc chuối nghiền nát để uống cùng. Khi đó, phải cho toàn bộ lượng thuốc vào khoảng một thìa nhỏ nước sinh tố táo, cháo, sữa chua hoặc chuối nghiền nát ở nhiệt độ phòng và phải uống ngay với nước. Lượng thuốc đã trộn với nước sinh tố táo, cháo hoặc sữa chua ổn định trong khoảng 6 giờ khi bảo quản trong tủ lạnh (2°C - 8°C/35°F - 45°F). Không được bảo quản trong tủ lạnh lượng thuốc đã trộn với chuối nghiền nát mà phải uống ngay.
Suy gan: Không cần điều chỉnh liều trên bệnh nhân suy gan nhẹ (Child-Pugh nhóm A). Dùng celecoxib theo liều bằng một nửa liều khuyến cáo cho các bệnh nhân viêm khớp hoặc bị đau trong suy gan vừa (Child-Pugh nhóm B).
Chưa có các nghiên cứu trên bệnh nhân suy gan nặng (Child-Pugh nhóm C) (xem phần Tác động trên gan).
Suy thận: Không cần chỉnh liều với các bệnh nhân suy thận vừa và nhẹ. Chưa có các nghiên cứu lâm sàng trên các bệnh nhân suy thận nặng (xem phần Tác động trên thận).
Dùng kết hợp với fluconazol: Nên dùng celecoxib với liều bằng một nửa liều khuyến cáo trên những bệnh nhân đang điều trị với fluconazol, một chất ức chế CYP2C9. Cần thận trọng khi dùng kết hợp celecoxib với các chất ức chế CYP2C9 (xem Tương tác với các thuốc khác và các dạng tương tác khác).
Không sử dụng trong trường hợp sau (Chống chỉ định)
Celecoxib chống chỉ định đối với:
- Bệnh nhân có tiền sử quá mẫn với celecoxib hoặc bất kỳ thành phần nào của thuốc.
- Bệnh nhân có tiền sử quá mẫn với sulfonamid
- Các bệnh nhân có tiền sử hen, mề đay hoặc có các phản ứng kiểu dị ứng sau khi dùng acid acetylsalicylic (ASA [aspirin]) hoặc các thuốc chống viêm không steroid khác (các NSAID), bao gồm các thuốc ức chế đặc hiệu cyclooxygenase - 2 (COX-2) khác.
- Điều trị đau trong phẫu thuật ghép mạch động mạch vành nhân tạo (CABG) (xem phần Cảnh báo và thận trọng đặc biệt khi sử dụng).
Lưu ý khi sử dụng (Cảnh báo và thận trọng)
Các tác động trên tim mạch
Huyết khối tim mạch: Celecoxib có thể gây tăng nguy cơ huyết khối tim mạch nghiêm trọng, nhồi máu cơ tim, và đột quỵ, những biến cố này có thể gây tử vong. Tất cả các NSAID đều có thể có chung nguy cơ này. Nguy cơ này có thể tăng theo liều dùng, thời gian dùng và các yếu tố nguy cơ tim mạch của bản thân. Bệnh nhân với tiền sử bệnh tim mạch có thể có nguy cơ cao hơn. Để giảm thiểu nguy cơ xảy ra tác dụng không mong muốn trên tim mạch ở bệnh nhân điều trị với celecoxib, nên dùng liều thấp nhất có hiệu quả trong thời gian ngắn nhất có thể. Thầy thuốc và bệnh nhân cần cảnh giác với sự phát triển của các trường hợp này, ngay cả khi không có các triệu chứng về tim mạch trước đó. Bệnh nhân cần được thông báo về các dấu hiệu và triệu chứng của các độc tính nghiêm trọng trên tim mạch và các bước phải làm khi chúng xảy ra (xem phần Các đặc tính dược lực học).
2 thử nghiệm lâm sàng lớn, có đối chứng về một NSAID tác động chọn lọc trên COX-2 khác trong điều trị đau 10 - 14 ngày đầu sau khi phẫu thuật ghép mạch động mạch vành nhân tạo (CABG) cho thấy có sự tăng tỷ lệ nhồi máu cơ tim và đột quỵ (xem phần Chống chỉ định).
Celecoxib không phải là một chất thay thế cho acid acetylsalicylic trong dự phòng các bệnh tắc nghẽn huyết khối tim mạch do thiếu tác động trên chức năng tiểu cầu. Bởi vì celecoxib không ức chế sự kết tập tiểu cầu, không nên ngừng các trị liệu kháng tiểu cầu (ví dụ acid acetylsalicylic).
Tăng huyết áp: Cũng như tất cả các NSAID, celecoxib có thể làm khởi phát cơn tăng huyết áp hoặc làm tình trạng tăng huyết áp vốn có nặng thêm, cả hai yếu tố này đều có thể làm tăng biến cố tim mạch. Nên thận trọng khi dùng các NSAID, kể cả celecoxib trên bệnh nhân tăng huyết áp. Cần theo dõi huyết áp chặt chẽ khi bắt đầu điều trị với celecoxib cũng như trong suốt thời gian điều trị.
Ứ dịch và phù: Cũng giống như các thuốc có tác dụng ức chế tổng hợp prostaglandin, phù nề và ứ dịch đã gặp trên một số bệnh nhân dùng celecoxib. Do đó, cần theo dõi chặt chẽ bệnh nhân bị suy tim sung huyết hoặc tăng huyết áp từ trước. Nên dùng celecoxib thận trọng cho các bệnh nhân đã bị tổn thương chức năng tim, phù hoặc các tình trạng có khả năng trở nên trầm trọng hơn do ứ dịch và phù bao gồm những người dùng thuốc lợi tiểu, hoặc có nguy cơ giảm thể tích máu.
Các tác động trên đường tiêu hóa
Thủng đường tiêu hóa trên và dưới, loét hoặc chảy máu đã xảy ra với các bệnh nhân dùng celecoxib. Những bệnh nhân có nguy cơ cao nhất bị những biến chứng đường tiêu hóa loại này khi dùng các thuốc NSAID bao gồm: người cao tuổi, bệnh nhân bị các bệnh tim mạch, bệnh nhân đang dùng aspirin, các glucocorticoid hoặc các NSAID khác, bệnh nhân dùng thức uống có cồn hoặc bệnh nhân có tiền sử hoặc đang bị các bệnh đường tiêu hóa tiến triển như loét, các tình trạng chảy máu hoặc viêm đường tiêu hóa. Hầu hết các báo cáo ngẫu nhiên về các trường hợp tử vong do biến cố trên đường tiêu hoá có liên quan đến celecoxib là trên các bệnh nhân thể chất yếu hoặc người cao tuổi.
Các tác động trên thận
Các NSAID bao gồm celecoxib có thể gây độc cho thận. Các thử nghiệm lâm sàng với celecoxib đã chỉ ra các tác động tương tự như với các NSAID khác được so sánh. Bệnh nhân có nguy cơ nhiễm độc thận cao nhất là người suy chức năng thận, suy tim, suy chức năng gan và người cao tuổi. Cần theo dõi cẩn thận những bệnh nhân này khi điều trị bằng celecoxib.
Cần thận trọng khi bắt đầu điều trị cho bệnh nhân bị mất nước. Trước tiên nên bù nước cho bệnh nhân rồi mới bắt đầu điều trị bằng celecoxib.
Bệnh thận tiến triển
Cần theo dõi chặt chẽ chức năng thận ở bệnh nhân bị bệnh thận tiến triển dùng celecoxib (xem phần Liều dùng và cách dùng).
Phản ứng phản vệ
Cũng như các thuốc NSAID nói chung, các phản ứng phản vệ đã xảy ra trên các bệnh nhân dùng celecoxib (xem phần Chống chỉ định).
Các phản ứng nghiêm trọng trên da
Các phản ứng nghiêm trọng trên da, một số dẫn đến tử vong, bao gồm viêm da tróc vẩy, hội chứng Steven-Johnson, và hoại tử biểu bì nhiễm độc, đã được báo cáo nhưng rất hiếm gặp trong sử dụng celecoxib. Bệnh nhân thường có nguy cơ cao với các biến cố này trong giai đoạn sớm của quá trình điều trị, các trường hợp này xảy ra chủ yếu trong tháng đầu tiên dùng thuốc, cần ngưng dùng celecoxib ngay khi xuất hiện mẩn đỏ da, tổn thương niêm mạc, hoặc bất kỳ dấu hiệu quá mẫn nào.
Các tác động trên gan
Chưa có nghiên cứu trên các bệnh nhân suy gan nặng (Child-Pugh nhóm C). Không sử dụng celecoxib trên các bệnh nhân suy gan nặng. Celecoxib cần được sử dụng thận trọng trên các bệnh nhân suy gan vừa (Child - Pugh nhóm B), và nên bắt đầu với liều bằng một nửa liều khuyến cáo (xem phần Liều dùng và cách dùng).
Các tác dụng không mong muốn nghiêm trọng hiếm gặp trên gan, bao gồm viêm gan kịch phát (một số trường hợp gây tử vong), hoại tử gan và suy gan (một số trường hợp gây tử vong hoặc cần phải ghép gan) đã được báo cáo với celecoxib.
Bệnh nhân có các triệu chứng và/hoặc dấu hiệu của suy gan hoặc người có xét nghiệm chức năng gan bất thường cần được theo dõi chặt chẽ về các dấu hiệu phát triển phản ứng trên gan trầm trọng hơn trong quá trình điều trị với celecoxib.
Sử dụng đồng thời với thuốc chống đông máu đường uống
Việc sử dụng đồng thời các NSAID với thuốc chống đông máu đường uống làm tăng nguy cơ xuất huyết và cần được sử dụng thận trọng. Các thuốc chống đông máu đường uống bao gồm các thuốc dạng warfarin/coumarin và các thuốc chống đông máu đường uống thế hệ mới (ví dụ: apixaban, dabigatran và rivaroxaban). Đã có báo cáo về trường hợp chảy máu nghiêm trọng trên các bệnh nhân đang dùng đồng thời với warfarin hoặc các chất tương tự, trong đó có một số trường hợp gây tử vong. Do đã có báo cáo về tăng thời gian prothrombin (INR), tác dụng chống đông/INR cần được theo dõi ở những bệnh nhân dùng thuốc chống đông dạng warfarin/coumarin hoặc chỉnh liều sau khi bắt đầu điều trị bằng celecoxib (xem phần Tương tác với các thuốc khác và các dạng tương tác khác).
Tổng quan
Với tác dụng giảm viêm, celecoxib có thể làm mờ các dấu hiệu chẩn đoán, ví dụ như triệu chứng sốt trong chẩn đoán nhiễm trùng.
Cần tránh dùng đồng thời celecoxib với một thuốc NSAID không phải aspirin.
Ức chế CYP 2D6
Celecoxib cho thấy có khả năng ức chế CYP2D6 ở mức trung bình. Đối với những thuốc được chuyển hóa bởi CYP2D6, có thể cần phải giảm liều trong thời gian bắt đầu điều trị bằng celecoxib hoặc tăng liều khi ngưng điều trị bằng celecoxib (xem phần Tương tác với các thuốc khác và các dạng tương tác khác).
Tác dụng không mong muốn (Tác dụng phụ)
Dữ liệu trong các thử nghiệm lâm sàng
Các tác dụng không mong muốn (ADR) trong Bảng 1 được báo cáo với tỉ lệ lớn hơn 0,01% ở nhóm dùng celecoxib và cao hơn so với báo cáo ở nhóm dùng giả dược, trong 12 thử nghiệm lâm sàng có đối chứng với giả dược và/hoặc với hoạt chất khác, kéo dài tới 12 tuần, dùng liều hàng ngày từ 100mg đến 800mg ở người lớn. Tần suất của các ADR trong Bảng 1 được cập nhật dựa trên dữ liệu tổng hợp từ 89 thử nghiệm lâm sàng ngẫu nhiên có đối chứng mô tả việc sử dụng trên lâm sàng ở 38.102 bệnh nhân dùng celecoxib. Tần suất ADR được định nghĩa như sau: rất thường gặp (> 10%), thường gặp (> 1% và < 10%), ít gặp (> 0,1% và < 1%), hiếm gặp (> 0,01% và < 0,1%), rất hiếm gặp (< 0,01%). Các ADR trong Bảng 1 được liệt kê theo hệ cơ quan và xếp thứ tự theo tần suất giảm dần.
|
Bảng 1. Tác dụng không mong muốn của thuốc (ADR) trong 12 thử nghiệm lâm sàng có đối chứng với giả dược và/hoặc với hoạt chất khác, và tần suất ADR từ 89 thử nghiệm lâm sàng ngẫu nhiên, có đối chứng về đau và viêm với liều hàng ngày từ 25mg - 800mg ở nhóm đối tượng người trưởng thành
|
|
Hệ cơ quan
|
Tác dụng không mong muốn
|
|
Tần suất
|
|
|
Nhiễm trùng
|
|
Thường gặp
|
Viêm phế quản, viêm xoang, nhiễm khuẩn đường hô hấp trên, nhiễm khuẩn đường tiết niệu
|
|
Ít gặp
|
Viêm họng, viêm mũi
|
|
Rối loạn máu và hệ bạch huyết
|
|
Ít gặp
|
Thiếu máu
|
|
Hiếm gặp
|
Giảm tiểu cầu
|
|
Rối loạn hệ miễn dịch
|
|
Ít gặp
|
Quá mẫn
|
|
Rối loạn tâm thần
|
|
Thường gặp
|
Mất ngủ
|
|
Ít gặp
|
Lo lắng
|
|
Hiếm gặp
|
Trạng thái lú lẫn
|
|
Rối loạn thần kinh
|
|
Thường gặp
|
Chóng mặt
|
|
Ít gặp
|
Tăng trương lực cơ, buồn ngủ
|
|
Rối loạn mắt
|
|
Ít gặp
|
Nhìn mờ
|
|
Rối loạn tai và tai trong
|
|
Không thường gặp
|
Ù tai
|
|
Rối loạn tim
|
|
Ít gặp
|
Tim đập nhanh
|
|
Hiếm gặp
|
Suy tim sung huyết, loạn nhịp, tim đập nhanh
|
|
Rối loạn mạch máu
|
|
Thường gặp
|
Tăng huyết áp (bao gồm cả tăng huyết áp nặng hơn)
|
|
Hiếm gặp
|
Đỏ mặt
|
|
Rối loạn hô hấp, vùng ngực và trung thất
|
|
Thường gặp
|
Ho
|
|
Rối loạn tiêu hóa
|
|
Thường gặp
|
Nôn mửa, đau bụng, tiêu chảy, khó tiêu, đầy bụng
|
|
Ít gặp
|
Loét dạ dày, rối loạn về răng
|
|
Hiếm gặp
|
Loét tá tràng, loét thực quản
|
|
Rất hiếm gặp
|
Thủng ruột, viêm tụy
|
|
Rối loạn gan mật
|
|
Ít gặp
|
Men gan tăng (bao gồm cả tăng alanin aminotransferase và tăng aspartat aminotransferase)
|
|
Rối loạn da và mô dưới da
|
|
Thường gặp
|
Ngứa (bao gồm cả ngứa toàn thân), phát ban
|
|
Ít gặp
|
Mày đay, bầm máu
|
|
Hiếm gặp
|
Phù mạch, rụng tóc
|
|
Rất hiếm gặp
|
Viêm da bọng nước
|
|
Rối loạn toàn thân và tại chỗ
|
|
Thường gặp
|
Phù ngoại biên
|
|
Ít gặp
|
Phù mặt, bệnh giống cúm
|
|
Tổn thương, nhiễm độc và tình trạng do thủ thuật
|
|
Ít gặp
|
Tổn thương
|
Các tác dụng không mong muốn của thuốc* thêm vào trong Bảng 2 dưới đây được báo cáo với tỉ lệ xảy ra lớn hơn so với giả dược trong nghiên cứu phòng ngừa polyp kéo dài tới 3 năm với liều hàng ngày từ 400mg đến 800mg (xem phần An toàn trên tim mạch – Thử nghiệm dài ngày trên bệnh nhân bị polyp u tuyến rải rác). Tần suất của ADR trong Bảng 2 được xác định dựa trên các nghiên cứu phòng ngừa polyp lâu dài này và được định nghĩa: rất thường gặp (> 10%), thường gặp (> 1% và < 10%), ít gặp (> 0,1% và < 1%). Các ADR trong Bảng 2 được liệt kê theo hệ cơ quan và xếp thứ tự theo tần suất giảm dần.
| Bảng 2. Tác dụng không mong muốn của thuốc trong nghiên cứu phòng ngừa polyp kéo dài tới 3 năm với liều hàng ngày từ 400mg - 800mg |
|
Hệ cơ quan
|
Tác dụng không mong muốn |
|
Tần suất
|
|
Nhiễm trùng
|
|
Thường gặp
|
Nhiễm khuẩn tai, nhiễm nấm**
|
|
Ít gặp
|
Nhiễm Helicobacter, Herpes zoster, viêm quầng, nhiễm khuẩn vết thương, viêm lợi, viêm tai trong, nhiễm khuẩn
|
|
U tân sinh lành tính, ác tính, và chưa phân loại
|
|
Ít gặp
|
u mỡ
|
|
Rối loạn tâm thần
|
|
Ít gặp
|
Rối loạn giấc ngủ
|
|
Rối loạn thần kinh
|
|
Ít gặp
|
Nhồi máu não
|
|
Rối loạn mắt
|
|
Ít gặp
|
Xuất huyết kết mạc, thấy đốm đen bay trước mắt (vitreous floaters)
|
|
Rối loạn tai và tai trong
|
|
Ít gặp
|
Giảm thính lực
|
|
Rối loạn tim
|
|
Thường gặp
|
Nhồi máu cơ tim, đau thắt ngực
|
|
Ít gặp
|
Đau thắt ngực thể không ổn định, thiểu năng van động mạch, xơ vữa động mạch vành, nhịp tim chậm xoang, phì đại tâm thất
|
|
Rối loạn mạch máu
|
|
Rất thường gặp
|
Tăng huyết áp*
|
|
Ít gặp
|
Huyết khối tĩnh mạch sâu, tụ máu
|
|
Rối loạn hô hấp, vùng ngực và trung thất
|
|
Thường gặp
|
Khó thở
|
|
Ít gặp
|
Khó phát âm
|
|
Rối loạn tiêu hóa
|
|
Rất thường gặp
|
Tiêu chảy*
|
|
Thường gặp
|
Nôn mửa*, khó nuốt, hội chứng ruột kích thích, bệnh trào ngược dạ dày thực quản, buồn nôn, chi nang
|
|
Ít gặp
|
Trĩ xuất huyết, ruột co bóp thường xuyên, loét miệng, viêm dạ dày
|
|
Rối loạn gan mật
|
|
Thường gặp
|
Men gan tăng (bao gồm cả tăng alanin aminotransferase và tăng aspartat aminotransferase)*
|
|
Rối loạn da và mô dưới da
|
|
Ít gặp
|
Viêm da dị ứng
|
|
Rối loạn cơ xương và mô liên kết
|
|
Thường gặp
|
Co thất cơ
|
|
Ít gặp
|
U nang bao hoạt dịch
|
|
Rối loạn thận và tiết niệu
|
|
Thường gặp
|
Sỏi thận
|
|
Ít gặp
|
Đi tiểu đêm
|
|
Rối loạn tuyến vú và hệ sinh sản
|
|
Thường gặp
|
Xuất huyết âm đạo, viêm tiền liệt tuyến, tăng sản tiền liệt tuyến lành tính
|
|
Ít gặp
|
Nang buồng trứng, các triệu chứng tắt kinh, căng ngực, thống kinh
|
|
Rối loạn toàn thân và tại chỗ
|
|
Ít gặp
|
Phù
|
|
Thăm khám
|
|
Thường gặp
|
Tăng creatinin máu, tăng kháng nguyên đặc hiệu tiền liệt, tăng cân
|
|
Ít gặp
|
Tăng kali máu, tăng natri máu, giảm testosteron máu, giảm tỷ lệ hồng cầu, tăng hemoglobin
|
|
Tổn thương, nhiễm độc và các biến chứng do thủ thuật
|
|
Ít gặp
|
Gẫy bàn chân, gẫy chi dưới, gẫy xương, viêm mỏm gò xương, đứt gân
|
* Tăng huyết áp, nôn mửa, tiêu chảy và tăng men gan được liệt kê trong Bảng 2 vì những biến cố này có tần suất cao hơn trong các nghiên cứu kéo dài tới 3 năm, so với Bảng 1 bao gồm những tác dụng không mong muốn trong các nghiên cứu chỉ kéo dài 12 tuần.
** Chủ yếu là nhiễm nấm tại chỗ.
Các tác dụng không mong muốn được báo cáo sau khi đưa thuốc ra thị trường
Các tác dụng không mong muốn xác định được sau khi đưa thuốc ra thị trường được trình bày dưới đây. Mặc dù các phản ứng này được xác định từ các báo cáo sau lưu hành, dữ liệu thử nghiệm đã được tham khảo để ước tính tần suất. Như đã nêu trên, tần suất được dựa trên tập hợp các thử nghiệm mô tả việc dùng thuốc trên 38.102 bệnh nhân. Tần suất được định nghĩa như sau: rất thường gặp (> 10%); thường gặp (> 1% và < 10%), ít gặp (> 0,1% và < 1%), hiếm gặp (> 0,01% va < 0,1%), rất hiếm gặp (< 0,01%), không rõ (không thể ước lượng từ dữ liệu có sẵn).
Rối loạn hệ miễn dịch: Rất hiếm gặp: phản ứng phản vệ.
Rối loạn tâm thần: Hiếm gặp: ảo giác
Rối loạn thần kinh: Rất hiếm gặp: xuất huyết não, viêm màng não vô khuẩn, mất vị giác, mất khứu giác.
Rối loạn mắt: Ít gặp: viêm kết mạc
Rối loạn mạch máu: Rất hiếm gặp: viêm mạch.
Rối loạn hô hấp, vùng ngực và trung thất: Hiếm gặp: nghẽn mạch phổi, viêm phổi.
Rối loạn tiêu hóa: Hiếm gặp: xuất huyết tiêu hóa
Rối loạn gan mật: Hiếm gặp: viêm gan; Rất hiếm gặp: suy gan, viêm gan kịch phát, hoại tử gan (xem phần các tác động trên gan) ứ mật, viêm gan tắc mật, bệnh vàng da
Rối loạn da và mô dưới da: Hiếm gặp: phản ứng nhạy cảm với ánh sáng; Rất hiếm gặp: hội chứng Stevens-Johnson, hồng ban đa dạng, hoại tử biểu bì nhiễm độc, phản ứng do thuốc kèm theo tăng bạch cầu ưa eosin và các triệu chứng toàn thân (DRESS hoặc hội chứng quá mẫn), ngoại ban mụn mủ toàn thân cấp tính (AGEP), viêm da tróc vảy.
Rối loạn thận và tiết niệu: Hiếm gặp: suy thận cấp (xem phần Các tác động trên thận), giảm natri máu; Rất hiếm gặp: viêm thận kẽ, hội chứng thận hư, viêm cầu thận sang thương tối thiểu.
Rối loạn tuyến vú và hệ sinh sản: Hiếm gặp: rối loạn kinh nguyệt; Chưa xác định được: rối loạn khả năng sinh sản ở nữ giới (bệnh suy giảm khả năng sinh sản ở nữ giới) (xem phần Ảnh hưởng trên khả năng sinh sản, phụ nữ có thai và cho con bú).
Rối loạn toàn thân và tại chỗ: Ít gặp: đau ngực
Phụ nữ có ý định mang thai được loại khỏi tất cả các thử nghiệm, do đó tham khảo cơ sở dữ liệu thử nghiệm về tần suất của trường hợp này là không hợp lý.
Tương tác với các thuốc khác
Tổng quan
Celecoxib chủ yếu chuyển hóa qua cytocrom P450 (CYP) 2C9 tại gan. Cần thận trọng khi dùng celecoxib trên bệnh nhân đã biết hoặc nghi ngờ chuyển hóa qua CYP2C9 kém dựa trên tiền sử với các cơ chất khác của CYP2C9 vì nồng độ thuốc trong huyết tương có thể cao bất thường do giảm độ thanh thải chuyển hóa. Nên bắt đầu điều trị với liều bằng một nửa liều khuyến nghị (xem phần Liều lượng và cách dùng và Chuyển hóa).
Việc sử dụng đồng thời celecoxib với các chất ức chế CYP2C9 có thể dẫn đến việc tăng nồng độ celecoxib trong huyết tương. Vì vậy, có thể cần giảm liều celecoxib khi celecoxib được sử dụng đồng thời với các chất ức chế CYP2C9.
Việc sử dụng celecoxib đồng thời với các chất cảm ứng CYP2C9 như rifampicin, carbamazepin và barbiturat có thể dẫn đến việc giảm nồng độ celecoxib trong huyết tương. Vì vậy, có thể cần tăng liều celecoxib khi celecoxib được sử dụng đồng thời với các chất cảm ứng CYP2C9.
Nghiên cứu dược động học và nghiên cứu in vitro cho thấy mặc dù celecoxib không phải là cơ chất nhưng nó có tác dụng ức chế CYP2D6. Do đó có thể có tương tác in vitro giữa celecoxib với các thuốc chuyển hóa bởi CYP2D6.
Với các thuốc cụ thể
Tương tác giữa celecoxib và warfarin hoặc các thuốc tương tự: (xem phần Sử dụng đồng thời với thuốc chống đông máu đường uống).
Lithium: Ở đối tượng khỏe mạnh, nồng độ lithium trong huyết tương tăng khoảng 17% khi dùng đồng thời lithium và celecoxib. Cần theo dõi chặt chẽ bệnh nhân đang điều trị bằng lithium khi dùng celecoxib hoặc ngừng dùng celecoxib.
Aspirin: Celecoxib không ảnh hưởng đến tác động kháng tiểu cầu của aspirin liều thấp (xem phần Các tác động trên đường tiêu hóa). Vì không có tác động trên tiểu cầu, celecoxib không phải là chất thay thế cho aspirin trong điều trị dự phòng bệnh tim mạch.
Các thuốc chống tăng huyết áp bao gồm các chất ức chế men chuyển angiotensin (ACEI), chất đối kháng angiotensin II (còn được gọi là thuốc chẹn thụ thể angiotensin, ARB), các thuốc lợi tiểu và các thuốc chẹn beta: Việc ức chế prostaglandin có thể làm giảm tác dụng của các thuốc chống tăng huyết áp bao gồm ACEI và/hoặc ARB, thuốc lợi tiểu và thuốc chẹn beta, cần lưu ý tương tác này khi dùng đồng thời celecoxib với ACEI và/hoặc ARB, thuốc lợi tiểu và thuốc chẹn beta.
Đối với bệnh nhân cao tuổi, bị giảm thể dịch (bao gồm cả những người đang dùng thuốc lợi tiểu) hoặc bị tổn thương chức năng thận, việc dùng đồng thời thuốc NSAID, bao gồm thuốc ức chế chọn lọc COX-2, với thuốc ức chế men chuyển angiotensin, các chất đối kháng angiotensin II hoặc thuốc lợi tiểu có thể dẫn đến tổn hại chức năng thận bao gồm suy thận cấp tính. Các tác dụng này thường có thể phục hồi. Vì vậy, cần thận trọng khi sử dụng đồng thời những thuốc này. Cần cho bệnh nhân uống nước đầy đủ và về mặt lâm sàng cần theo dõi, đánh giá chức năng thận khi bắt đầu điều trị kết hợp và đánh giá theo định kỳ sau đó.
Kết quả từ nghiên cứu lisinopril: Trong một nghiên cứu lâm sàng kéo dài 28 ngày ở bệnh nhân tăng huyết áp giai đoạn I và II đối chứng bằng lisinopril, kết quả của việc sử dụng celecoxib 200mg hai lần mỗi ngày cho thấy huyết áp tâm thu hoăc tâm trương trung bình hằng ngày, được xác định bằng phương pháp theo dõi huyết áp lưu động 24 giờ, không tăng có ý nghĩa về mặt lâm sàng khi so sánh với điều trị bằng giả dược. Trong những bệnh nhân sử dụng đồng thời với celecoxib 200mg hai lần mỗi ngày, 48% được xem là không đáp ứng với lisinopril vào lần thăm khám cuối cùng (nghĩa là huyết áp tâm trương >90mmHg hoặc huyết áp tâm trương tăng >10% so với mức cơ sở), so với 27% ở bệnh nhân sử dụng đồng thời với giả dược; sự khác biệt này có ý nghĩa về mặt thống kê.
Cyclosporin: Do có tác dụng trên prostaglandin thận, các NSAID có thể làm tăng nguy cơ nhiễm độc thận do cyclosporin.
Fluconazol và ketoconazol: Dùng đồng thời fluconazol liều 200mg, 1 lần/ngày làm tăng gấp đôi nồng độ celecoxib trong huyết tương. Việc tăng lên này là do tác động ức chế sự chuyển hóa của celecoxib qua CYP P450 2C9 bởi fluconazol. Celecoxib nên được sử dụng với liều bằng một nửa liều khuyến cáo ở bệnh nhân đang dùng fluconazol, một chất ức chế CYP2C9 (xem phần Liều dùng và cách dùng). Ketoconazol, một chất ức chế CYP3A4, không có tác dụng ức chế chuyển hóa celecoxib đáng kể trên lâm sàng.
Dextromethorphan và metoprolol: Sử dụng đồng thời celecoxib 200mg hai lần mỗi ngày dẫn đến việc tăng lần lượt 2,6 lần và 1,5 lần nồng độ dextromethorphan và metoprolol trong huyết tương (cơ chất của CYP2D6). Việc tăng lên này là do sự ức chế của celecoxib lên sự chuyển hóa cơ chất của CYP2D6 qua CYP2D6. Vì vậy, có thể cần giảm liều lượng của các thuốc là cơ chất của CYP2D6 khi bắt đầu điều trị bằng celecoxib hoặc tăng liều khi ngưng điều trị bằng celecoxib (xem phần Sử dụng đồng thời với thuốc chống đông máu đường uống).
Thuốc lợi tiểu: Các nghiên cứu lâm sàng cho thấy trên một số bệnh nhân, NSAID có thể làm giảm tác dụng tăng thải natri qua nước tiểu của furosemid và thiazid bằng cách ức chế tổng hợp prostaglandin.
Methotrexat: Không quan sát thấy tương tác dược động học nào trong nghiên cứu lâm sàng giữa celecoxib và methotrexat.
Các thuốc tránh thai đường uống: Trong một nghiên cứu tương tác, celecoxib không có tác động rõ ràng trên lâm sàng với dược động học của thuốc tránh thai đường uống loại kết hợp (1mg norethindrone/0,035mg ethinyl estradiol)
Các thuốc khác: Chưa có báo cáo tương tác quan trọng nào về mặt lâm sàng giữa celecoxib và thuốc kháng acid (nhôm và magnesi), omeprazol, glibenclamid (glyburid), phenytoin hoặc tolbutamid.
Quá liều
Dữ liệu lâm sàng về tình trạng quá liều còn hạn chế. Dùng liều đơn 1200mg hoặc đa liều với tổng liều là 1200 mg/ngày trên người khỏe mạnh không cho thấy tác dụng không mong muốn nào có ý nghĩa về mặt lâm sàng. Trong trường hợp nghi ngờ quá liều, nên có các biện pháp hỗ trợ về y tế thích hợp. Thẩm phân máu không phải là biện pháp hiệu quả để loại bỏ thuốc vì thuốc liên kết mạnh với protein.
Thai kỳ và cho con bú
Ảnh hưởng trên khả năng sinh sản
Dựa trên cơ chế hoạt động, việc sử dụng các NSAID, kể cả celecoxib có thể gây trì hoãn hoặc ngăn cản sự rụng trứng, liên quan đến hiện tượng vô sinh có thể phục hồi ở một số phụ nữ. Những phụ nữ khó thụ thai hay đang chữa vô sinh, cần cân nhắc việc ngừng dùng các NSAID, bao gồm cả celecoxib.
Phụ nữ có thai
Chưa có nghiên cứu trên phụ nữ có thai. Một số nghiên cứu trên động vật cho thấy có độc tính trên sinh sản (xem phần Các dữ liệu an toàn tiền lâm sàng). Chưa có các dữ liệu tương đương trên người.
Celecoxib, cũng như các thuốc ức chế tổng hợp prostaglandin khác, có thể gây vô lực cơ tử cung và đóng sớm ống động mạch chủ, không nên dùng celecoxib vào 3 tháng cuối của thai kỳ.
Chỉ nên dùng celecoxib khi mang thai nếu lợi ích có thể có đối với người mẹ vượt trội nguy cơ tiềm tàng đối với thai nhi.
Ức chế tổng hợp prostaglandin có thể gây ảnh hưởng bất lợi cho phụ nữ mang thai. Dữ liệu từ các nghiên cứu dịch tễ cho thấy nguy cơ sảy thai tự phát tăng lên sau khi dùng các thuốc ức chế tổng hợp prostaglandin trong giai đoạn sớm của thai kỳ. Dùng các thuốc ức chế tổng hợp prostaglandin trên động vật cho thấy nguy cơ sảy thai tăng lên ở giai đoạn trước và sau khi phôi làm tổ.
Phụ nữ cho con bú
Nghiên cứu trên chuột cho thấy celecoxib được bài tiết qua sữa với nồng độ tương đương với nồng độ trong huyết tương. Trên phụ nữ cho con bú dùng celecoxib, rất ít celecoxib xuất hiện trong sữa. Vì có thể có tác dụng không mong muốn của celecoxib trên trẻ đang bú mẹ, tùy theo lợi ích của thuốc với người mẹ, nên cân nhắc ngừng thuốc hay ngừng cho con bú.
Bảo quản
Bảo quản dưới 30°C. Lượng thuốc hòa tan trong nước sinh tố táo, cháo, sữa chua ổn định trong tối đa 6 giờ khi bảo quản trong tủ lạnh (2 - 8°C). Không được bảo quản lượng thuốc trộn lẫn trong chuối nghiền nát trong tủ lạnh mà phải uống luôn.
Quy cách đóng gói
Hộp 3 vỉ x 10 viên nang.
Hạn dùng
36 tháng kể từ ngày sản xuất.
Dược lực học
Nhóm trị liệu: M01AH Coxibs.
Cơ chế tác dụng của celecoxib là ức chế tổng hợp prostaglandin chủ yếu bằng cách ức chế cyclooxygenase-2 (COX-2). Ở nồng độ điều trị trên người, celecoxib không ức chế enzym cyclooxygenase-1 (COX-1). COX-2 được tạo ra nhằm đáp ứng với tác nhân gây viêm. Điều này dẫn đến việc tổng hợp và tích lũy các prostanoid gây viêm, đặc biệt là prostaglandin E2, gây viêm, phù nề và đau. Celecoxib tác dụng như một chất kháng viêm, giảm đau, và hạ nhiệt trên các mô hình động vật do ngăn cản quá trình sản xuất các prostanoid gây viêm thông qua ức chế COX-2. Trong các mô hình u ruột kết ở động vật, celecoxib giảm tỷ lệ và sự nhân lên của các khối u.
Các nghiên cứu in vitro và ex vivo cho thấy celecoxib có ái lực rất thấp với enzym COX-1. Vì vậy, ở liều điều trị, celecoxib không có tác dụng trên các prostanoid được tổng hợp do kích hoạt COX-1, do đó, không ảnh hưởng tới các quá trình sinh lý bình thường liên quan đến COX-1 ở mô, đặc biệt với dạ dày, ruột và tiểu cầu.
Dược động học
Hấp thu
Dược động học của celecoxib đã được đánh giá trên khoảng 1500 người. Khi dùng lúc đói celecoxib dễ dàng được hấp thu và đạt nồng độ đỉnh trong huyết tương sau khoảng 2 - 3 giờ. Sinh khả dụng đường uống dạng viên nang là 99% so với dạng hỗn dịch (dạng uống tối ưu hiện có). Khi được dùng lúc đói, cả nồng độ đỉnh trong huyết tương (Cmax) và diện tích dưới đường cong (AUC) đều tỷ lệ với liều cho đến 200mg, 2 lần/ngày; ở liều cao hơn, tỷ lệ tăng tương ứng của Cmax và AUC thấp hơn.
Phân bố
Tỷ lệ gắn kết với protein huyết tượng (tỷ lệ này không phụ thuộc nồng độ) là khoảng 97% ở nồng độ điều trị trong huyết tương và celecoxib không ưu tiên gắn với hồng cầu.
Chuyển hóa
Celecoxib được chuyển hóa chủ yếu qua cytocrom P450 2C9. Ba sản phẩm chuyển hóa không có tác dụng ức chế COX-1 hoặc COX-2 được nhận diện trong huyết thanh người là alcol bậc nhất, acid carboxylic tương ứng và liên hợp glucuronid của nó.
Hoạt tính của cytocrom P450 2C9 giảm ở người có đa hình di truyền và điều này dẫn đến giảm hoạt tính enzym, ví dụ người đồng hợp tử với đa hình CYP2C9*3.
Trong nghiên cứu dược động học với celecoxib 200mg dùng 1 lần/ngày ở người tình nguyện khỏe mạnh, kiểu gen là CYP2C9*1/*1, CYP2C9*1/*3,hoặc CYP2C9*3/*3, giá trị trung bình Cmax và AUC0-24 của celecoxib vào ngày 7 lần lượt là xấp xỉ gấp 4 lần và 7 lần, ở những người có kiểu gen CYP2C9*3/*3 so với các kiểu gen khác. Trong 3 nghiên cứu đơn liều riêng rẽ, có tổng cộng 5 đối tượng có kiểu gen CYP2C9*3/*3, giá trị AUC0-24 của liều đơn tặng khoảng 3 lần so với những người chuyển hóa bình thường. Ước tính tần suất xuất hiện của kiểu gen *3/*3 là 0,3% đến 1,0% ở các nhóm dân tộc khác nhau.
Bệnh nhân đã biết hoặc nghi ngờ có chuyển hóa CYP2C9 kém dựa trên tiền sử/kinh nghiệm với các cơ chất khác của CYP2C9 nên thận trọng khi dùng celecoxib. Nên xem xét việc bắt đầu điều trị với liều bằng một nửa liều khuyến nghị thấp nhất (Xem phần Liều dùng và cách dùng và Tương tác với các thuốc khác và các dạng tương tác khác).
Thải trừ
Celecoxib thải trừ chủ yếu do chuyển hóa qua gan với dưới 1% liều dùng được bài tiết nguyên dạng qua nước tiểu. Sau khi dùng đa liều, thời gian bán thải là 8 - 12 giờ và tốc độ thanh thải khoảng 500mL/phút. Với đa liều, nồng độ thuốc trong huyết tương đạt mức ổn định trước ngày thứ 5. Biến thiên giữa các đối tượng ở các thông số dược động học (AUC, Cmax, thời gian bán thải) là khoảng 30%. Thể tích phân bố ở trạng thái ổn định trung bình khoảng 500L/70kg ở người trưởng thành khỏe mạnh cho thấy sự phân bố rộng khắp của celecoxib vào các mô. Các nghiên cứu tiền lâm sàng đã xác định thuốc qua được hàng rào máu não.
Ảnh hưởng của thức ăn
Dùng thuốc cùng thức ăn (giàu chất béo) làm chậm sự hấp thu của celecoxib thể hiện qua Tmax đạt được sau khoảng 4 giờ và làm sinh khả dụng tăng khoảng 20% (xem phần Liều dùng và cách dùng).
Ở người tình nguyện khỏe mạnh, lượng hấp thu toàn thân (AUC) của celecoxib tương đương giữa dạng uống nguyên viên nang hoặc dạng hòa tan trong nước sốt táo. Không có sự thay đổi có ý nghĩa về Cmax, Tmax hoặc T1/2 sau khi uống thuốc nguyên viên hoặc hòa tan vào nước sốt táo.
Các nhóm bệnh nhân đặc biệt
Người cao tuổi
Ở người trên 65 tuổi, giá trị trung bình Cmax và AUC của celecoxib tăng lên 1,5 - 2 lần. Điều này chủ yếu liên quan đến cân nặng chứ không do thay đổi về tuổi tác, celecoxib có nồng độ cao hơn trên những bệnh nhân có cân nặng ít hơn và do đó cao hơn ở những người lớn tuổi có cân nặng trung bình thấp hơn những người trẻ. Do vậy, phụ nữ lớn tuổi có xu hướng có nồng độ thuốc trong huyết tương cao hơn đàn ông lớn tuổi. Nói chung không cần điều chỉnh liều. Tuy nhiên, với các bệnh nhân lớn tuổi có cân nặng dưới trung bình ( < 50kg), nên bắt đầu điều trị bằng liều khuyến nghị thấp nhất.
Chủng tộc
Một phân tích tổng hợp các nghiên cứu dược động học đã dự đoán AUC của celecoxib ở người da den cao hơn khoảng 40% so với người da trắng. Nguyên nhân và ý nghĩa lâm sàng của vấn đề này vẫn chưa được biết.
Suy gan
Nồng độ trong huyết tương của celecoxib ở bệnh nhân suy gan nhẹ (Child-Pugh Loại A) không có khác biệt đáng kể so với nồng độ ở nhóm đối chứng có tuổi và giới tính tương ứng. Trên các bệnh nhân suy gan vừa (Child-Pugh Loại B) nồng độ celecoxib trong huyết tương cao hơn khoảng 2 lần so với nhóm đối chứng tương ứng (xem phần Liều dùng và cách dùng).
Suy thận
Trên các bệnh nhân tình nguyện cao tuổi bị giảm tốc độ lọc cầu thận (GFR) do tuổi (GFR trung bình >65ml/phút/1,73m2) và các bệnh nhân bị suy thận mạn ổn định (GFR 35 - 60ml/phút/1,73m2), dược động học của celecoxib tương tự với các bệnh nhân có chức năng thận bình thường. Không có mối liên hệ đáng kể nào được tìm thấy giữa creatinin huyết thanh (hoặc hệ số thanh thải creatinin) và độ thanh thải celecoxib. Suy thận nặng không làm thay đổi độ thanh thải celecoxib do đường thải trừ chính của thuốc là qua chuyển hóa tại gan thành dạng không hoạt tính.
Ảnh hưởng trên thận
Các vai trò liên quan của COX-1 và COX-2 trong sinh lý thận chưa được biết đầy đủ. Celecoxib làm giảm sự thải trừ qua thận của PGE2 và 6-keto PGF1 α (một chất chuyển hóa của prostacyclin) nhưng không ảnh hưởng đến thải trừ thromboxan B2 huyết thanh và 11-dehydro-TXB2, một chất chuyển hóa của thromboxan (cả hai đều là sản phẩm của COX-1) Các nghiên cứu đặc thù đã cho thấy celecoxib không làm giảm GFR ở bệnh nhân lớn tuổi hoặc bệnh nhân suy thận mạn. Các nghiên cứu này cũng cho thấy có sự giảm bài tiết natri tạm thời. Trong các nghiên cứu trên các bệnh nhân viêm khớp, đã quan sát thấy tỷ lệ phù mạch ngoại vi tương đương so với bệnh nhân dùng các thuốc ức chế COX không đặc hiệu (cũng có tác động ức chế COX-2). Điều này thấy rõ nhất trên các bệnh nhân đang điều trị kết hợp với thuốc lợi tiểu. Tuy nhiên không ghi nhận tăng tỷ lệ của tăng huyết áp và suy tim; phù mạch ngoại vi thường nhẹ và tự hết.
Nghiên cứu tiền lâm sàng
Nghiên cứu lâm sàng
Thoái hoá khớp (Osteoarthritis - OA): Celecoxib đã được chứng minh có khả năng giảm đau khớp đáng kể so với giả dược. Celecoxib được đánh giá trong điều trị các dấu hiệu và triệu chứng của thoái hóa khớp gối và hông trên khoảng 4200 bệnh nhân trong thử nghiệm lâm sàng có đối chứng với giả dược và với hoạt chất khác trong thời gian tối đa 12 tuần. Ở những bệnh nhân thoái hóa khớp, điều trị bằng celecoxib 100mg hai lần mỗi ngày hoặc 200mg một lần mỗi ngày dẫn đến cải thiện được chỉ số WOMAC (Đại học Western Ontario và McMaster), là chỉ số tổng hợp các đại lượng đo lường về đau, cứng khớp và chức năng trong thoái hóa khớp. Trong ba nghiên cứu kéo dài 12 tuần về đau kèm theo bùng phát thoái hóa khớp, các liều celecoxib 100mg hai lần mỗi ngày hoặc 200mg hai lần mỗi ngày giúp giảm đau đáng kể trong vòng 24 - 48 giờ kể từ khi bắt đầu dùng thuốc. Ở mức liều 100mg hai lần mỗi ngày hoặc 200mg hai lần mỗi ngày, celecoxib đã được chứng minh có tính hiệu quả tương tự như naproxen 500mg hai lần mỗi ngày. Liều 200mg hai lần mỗi ngày không mang lại thêm lợi ích nào như đã thấy với liều 100mg hai lần mỗi ngày. Tổng liều lượng hàng ngày là 200mg đã được chứng minh là có hiệu quả như nhau cho dù dùng 100mg hai lần mỗi ngày hay 200mg một lần mỗi ngày.
Viêm khớp dạng thấp (Rheumatois arthritis - RAJ): Celecoxib đã được chứng minh có khả năng làm giảm tình trạng nhức/đau khớp và sưng khớp đáng kể so với giả dược. Celecoxib được đánh giá trong điều trị các dấu hiệu và triệu chứng của viêm khớp dạng thấp trên khoảng 2100 bệnh nhân trong thử nghiệm lâm sàng có đối chứng với giả dược và với hoạt chất khác trong thời gian tối đa 24 tuần. Celecoxib cho thấy hiệu quả vượt trội hơn giả dược trong các nghiên cứu này, bằng cách sử dụng Chỉ số đáp ứng 20 theo Hội Thấp khớp học Hoa Kỳ (American College of Rheumatology 20, ACR20), một chỉ số tổng hợp các đại lượng đo lường về lâm sàng, xét nghiệm và chức năng trong viêm khớp dạng thấp. Liều Celecoxib 100mg hai lần mỗi ngày và 200mg hai lần mỗi ngày có hiệu quả tương tự nhau và cả hai đều tương đương với naproxen 500mg hai lần mỗi ngày.
Mặc dù celecoxib 100mg hai lần mỗi ngày và 200mg hai lần mỗi ngày đều mang lại hiệu quả tổng thể tương tự nhau, nhưng một số bệnh nhân nhận được lợi ích lớn hơn từ liều 200mg hai lần mỗi ngày. Liều 400mg hai lần mỗi ngày không mang lại thêm lợi ích nào như đã thấy ở liều 100mg hay 200mg hai lần mỗi ngày.
Giảm đau, kể cả đau bụng kinh nguyên phát: Trong các mô hình giảm đau cấp tính đối với đau sau phẫu thuật răng miệng, đau sau phẫu thuật chấn thương chỉnh hình và đau bụng kinh nguyên phát, celecoxib làm giảm cơn đau từ vừa tới nặng theo đánh giá của bệnh nhân. Liều đơn trị celecoxib giúp giảm đau trong vòng 60 phút (xem phần Liều dùng và cách dùng).
Viêm cột sống dính khớp (Ankylosing spondylitis - AS): Celecoxib đã được đánh giá ở các bệnh nhân mắc viêm cột sống dính khớp trong hai thử nghiệm lâm sàng có đối chứng với giả dược và với hoạt chất khác (naproxen hoặc ketoprofen) trong thời gian 6 và 12 tuần. Celecoxib ở các liều 100mg hai lần mỗi ngày, 200mg một lần mỗi ngày và 400mg một lần mỗi ngày đã cho thấy tác dụng vượt trội về mặt thống kê so với giả dược trong các nghiên cứu này, đối với cả ba đại lượng chính cùng đánh giá tính hiệu quả bao gồm: đánh giá mức độ đau tổng thể (Thang điểm ước lượng trực quan), mức độ hoạt động tổng thể của bệnh (Thang điểm ước lượng trực quan) và suy giảm chức năng (Chỉ số chức năng viêm cột sống dính khớp Bath). Trong nghiên cứu kéo dài 12 tuần, không có sự khác biệt về mức độ cải thiện giữa liều 200mg và 400mg celecoxib khi so sánh mức độ thay đổi trung bình so với ban đầu, nhưng tỷ lệ bệnh nhân đáp ứng với celecoxib 400mg là 53%, lớn hơn so với celecoxib 200mg, là 44%, bằng phương pháp Đánh giá dựa trên tiêu chí đáp ứng trong viêm cột sống dính khớp (ASAS 20). ASAS 20 định nghĩa người đáp ứng là người đạt mức độ cải thiện so với ban đầu ít nhất 20% và mức độ cải thiện tuyệt đối ít nhất là 10mm, trên thang điểm từ 0 đến 100mm, ở ít nhất ba trong tổng số bốn yếu tố sau: đánh giá tổng thể bệnh nhân, đau, chỉ số chức năng viêm cột sống dính khớp Bath và viêm. Phân tích đáp ứng cũng cho thấy không có sự thay đổi nào về tỷ lệ đáp ứng khi vượt quá 6 tuần.
Thông tin thêm từ nghiên cứu lâm sàng
Nghiên cứu nội soi
Đánh giá nội soi đường tiêu hóa trên theo định kỳ được thực hiện trên hơn 4.500 bệnh nhân viêm khớp tham gia trong 5 thử nghiệm ngẫu nhiên có đối chứng kéo dài 12 - 24 tuần đối chứng với hoạt chất khác, 2 trong số các nghiên cứu này cũng có đối chứng bằng giả dược. Không có mối quan hệ nhất quán nào giữa tỷ lệ mắc viêm loét dạ dày tá tràng với liều celecoxib trong phạm vi nghiên cứu.
Bảng 3 tóm tắt tỷ lệ loét qua nội soi trong hai nghiên cứu 12 tuần trong đó bệnh nhân tham gia có kết quả nội soi ban đầu không phát hiện vết loét nào.
Bảng 3. Tỉ lệ loét dạ dày tá tràng từ các nghiên cứu nội soi ở bệnh nhân thoái hóa khớp và viêm khớp dạng thấp
| |
Nghiên cứu 3 tháng
|
| |
Nghiên cứu 1 (N = 1108)
|
Nghiên cứu 2 (N= 1049)
|
|
Giả dược
|
2,3% (5/217)
|
2,0% (4/200)
|
|
Celecoxib 50mg, 2 lần/ngày
|
3,4% (8/233)
|
...
|
|
Celecoxib 100mg, 2 lần/ngày
|
3,1% (7/227)
|
4,0% (9/223)
|
|
Celecoxib 200mg, 2 lần/ngày
|
5,9% (13/221)
|
2,7% (6/219)
|
|
Celecoxib 400mg, 2 lần/ngày
|
...
|
4,1% (8/197)
|
|
Naproxen 500mg, 2 lần/ngày
|
16,2% (34/210)*
|
17,6% (37/210)*
|
* p ≤ 0,05 so với tất cả các phương pháp điều trị khác.
Bảng 4 tóm tắt dữ liệu từ hai nghiên cứu 12 tuần trong đó bệnh nhân tham gia có kết quả nội soi ban đầu không phát hiện vết loét nào. Bệnh nhân đã thực hiện nội soi theo định kỳ 4 tuần một lần để cung cấp thông tin về nguy cơ loét theo thời gian.
Bảng 4. Tỉ lệ loét dạ dày tá tràng từ các nghiên cứu nội soi liên tiếp trong 3 tháng ở bệnh nhân thoái hóa khớp và viêm khớp dạng thấp
| |
Tuần 4
|
Tuần 8
|
Tuần 12
|
Tuần cuối cùng
|
|
Nghiên cứu 3 (N=523)
|
|
Celecoxib
|
4.0%
|
2.2%
|
1.5%
|
7.5%
|
|
200mg 2 lần/ngày
|
(10/252)*
|
(5/227)*
|
(3/196)*
|
(20/266)*
|
|
Naproxen
|
19.0%
|
14.2%
|
9.9%
|
34.6%
|
|
500mg 2 lần/ngày
|
(47/247)
|
(26/182)
|
(14/141)
|
(89/257)
|
|
Nghiên cứu 4 (N = 1062)
|
|
Celecoxib
|
3.9%
|
2.4%
|
1.8%
|
7.0%
|
|
200mg 2 lần/ngày
|
(13/337)+
|
(7/296) +
|
(5/274)+
|
(25/356)+
|
|
Diclofenac
|
5.1%
|
3.3%
|
2.9%
|
9.7%
|
|
75mg 2 lần/ngày
|
(18/350)
|
(10/306)
|
(8/278)
|
(36/372)
|
|
Ibuprofen
|
13.0%
|
6.2%
|
9.6%
|
23.3%
|
|
800mg 3 lần/ngày
|
(42/323)
|
(15/241)
|
(21/219)
|
(78/334)
|
*p ≤ 0,05 celecoxib so với naproxen dựa trên các phân tích theo định kì và tích lũy
+p ≤ 0,05 celecoxib so với ibuprofen dựa trên các phân tích theo định kỳ và tích lũy.
Một nghiên cứu ngẫu nhiên và mù đôi kéo dài 6 tháng trên 430 bệnh nhân viêm khớp dạng thấp đã được tiến hành, trong đó đã thực hiện kiểm tra nội soi vào thời điểm 6 tháng.
Tỷ lệ loét qua nội soi ở bệnh nhân dùng celecoxib 200mg hai lần mỗi ngày là 4%, so với 15% ở bệnh nhân dùng diclofenac SR 75mg hai lần mỗi ngày (p < 0,001).
Trong số 4 trên 5 nghiên cứu nội soi, khoảng 11% bệnh nhân (440/4000) có dùng aspirin (≤ 325mg/ngày). Ở nhóm dùng celecoxib, tỷ lệ loét qua nội soi ở những người sử dụng aspirin cao hơn so với người không sử dụng. Tuy nhiên, tỷ lệ gia tăng loét ở những người sử dụng aspirin thấp hơn so với tỷ lệ loét qua nội soi quan sát thấy ở các nhóm dùng hoạt chất so sánh, có dùng hoặc không dùng aspirin.
Chưa xác lập được mối tương quan nào giữa kết quả của nghiên cứu nội soi và tỷ lệ tương đối của các biến cố nghiêm trọng có ý nghĩa về mặt lâm sàng ở đường tiêu hoá trên. Xuất huyết đường tiêu hóa trên nghiêm trọng có ý nghĩa về mặt lâm sàng đã được quan sát thấy ở những bệnh nhân dùng celecoxib trong các thử nghiệm có đối chứng và nhãn mở, mặc dù không thường xuyên (xem phần Các tác động trên đường tiêu hóa)
Phân tích tổng hợp về tính an toàn trên đường tiêu hóa từ các nghiên cứu thoái hoá khớp và viêm khớp dạng thấp
Một phân tích dựa trên 31 nghiên cứu lâm sàng ngẫu nhiên có đối chứng về thoái hoá khớp và viêm khớp dạng thấp, bao gồm 39.605 bệnh nhân thoái hoá khớp (N = 25.903), viêm khớp dạng thấp (N = 3.232) hoặc những bệnh nhân mắc một trong hai tình trạng này (N = 10.470), và so sánh tỷ lệ mắc các tác dụng không mong muốn trên đường tiêu hoá ở bệnh nhân được điều trị bằng celecoxib với bệnh nhân dùng giả dược hoặc các NSAID khác (bao gồm cả naproxen, diclofenac và ibuprofen). Tỷ lệ loét trên lâm sàng và xuất huyết do loét khi dùng tổng liều hàng ngày celecoxib 200mg - 400mg là 0,2%, so với tỉ lệ 0,6% khi dùng các NSAID khác (RR = 0,35; CI 95% 0,22 - 0,56).
Nghiên cứu tính an toàn lâu dài của celecoxib trong điều trị Viêm xương khớp (nghiên cứu CLASS) bao gồm cả việc sử dụng cùng với aspirin:
Trong một nghiên cứu tiên cứu về kết quả an toàn dài hạn được tiến hành sau khi đưa thuốc ra thị trường ở khoảng 5.800 bệnh nhân mắc bệnh thoái hóa khớp và 2.200 bệnh nhân mắc bệnh viêm khớp dạng thấp, bệnh nhân đã dùng celecoxib 400mg hai lần mỗi ngày (lần lượt gấp 4 lần và gấp 2 lần liều khuyến cáo dùng cho thoái hóa khớp và viêm khớp dạng thấp), ibuprofen 800mg ba lần mỗi ngày hoặc diclofenac 75mg hai lần mỗi ngày (liều điều trị thông thường). Thời gian sử dụng trung bình với celecoxib (N = 3.987) và diclofenac (N = 1.996) là 9 tháng trong khi ibuprofen (N = 1.985) là 6 tháng. Tỷ lệ Kaplan-Meier tích lũy vào thời điểm 9 tháng được cung cấp cho tất cả các phân tích. Tiêu chí đánh giá chính của kết quả nghiên cứu này là tỷ lệ viêm loét có biến chứng (xuất huyết, thủng hoặc tắc nghẽn đường tiêu hóa). Bệnh nhân được phép dùng đồng thời aspirin (ASA) liều thấp (< 325mg/ngày) để phòng bệnh tim mạch (phân nhóm ASA: celecoxib, N = 882; diclofenac, N = 445; ibuprofen, N = 412). Sự khác biệt về tỷ lệ viêm loét có biến chứng giữa celecoxib và nhóm dùng kết hợp ibuprofen và diclofenac không có ý nghĩa về mặt thống kê. Những bệnh nhân dùng đồng thời celecoxib và ASA liều thấp có tỉ lệ viêm loét có biến chứng cao gấp 4 lần so với bệnh nhân không dùng ASA (xem phần Các tác động trên đường tiêu hóa).
Các kết quả về celecoxib được trình bày trong Bảng 5.
Bảng 5. Ảnh hưởng của việc dùng đồng thời Aspirin liều thấp lên tỷ lệ loét có biến chứng với Celecoxib 400mg 2 lần/ngày (tỷ lệ Kaplan-Meier ở 9 tháng [%])
| |
Người không dùng aspirin N = 3105
|
Người dùng aspirin N = 882
|
|
Loét có biến chứng
|
0,32
|
1,12
|
Chức năng tiểu cầu
Trên người tình nguyện khỏe mạnh, celecoxib ở các mức liều điều trị và ở các mức đa liều 600mg hai lần mỗi ngày (gấp ba lần so với liều khuyến cáo cao nhất) không gây ảnh hưởng trên quá trình kết tập tiểu cầu và thời gian xuất huyết khi so sánh với giả dược. Tất cả các nhóm đối chứng với hoạt chất khác (chất ức chế COX không đặc hiệu) đều thấy giảm đáng kể khả năng kết tập tiểu cầu và kéo dài thời gian xuất huyết (xem Hình 1).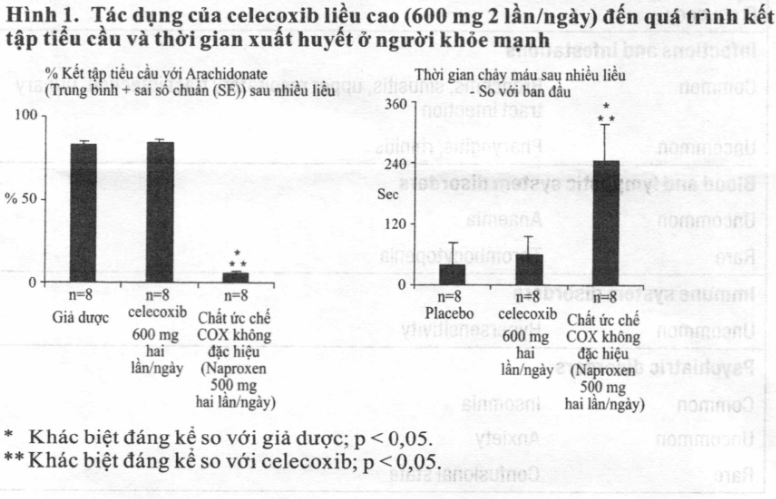 Nghiên cứu so sánh celecoxib với omeprazol và diclofenac trên những bệnh nhân có nguy cơ mắc thoái hoá khớp và viêm khớp dạng thấp (Nghiên cứu CONDOR)
Nghiên cứu so sánh celecoxib với omeprazol và diclofenac trên những bệnh nhân có nguy cơ mắc thoái hoá khớp và viêm khớp dạng thấp (Nghiên cứu CONDOR)
Trong nghiên cứu tiền cứu kéo dài 24 tuần ở bệnh nhân > 60 tuổi hoặc có tiền sử loét dạ dày tá tràng (trừ người sử dụng aspirin liều thấp), tỷ lệ phần trăm bệnh nhân gặp các biến cố về tiêu hóa (GI) có ý nghĩa về mặt lâm sàng (tiêu chí đánh giá tổng hợp chính) thấp hơn ở những bệnh nhân được điều trị bằng celecoxib 200mg hai lần/ngày so với những bệnh nhân được điều trị bằng diclofenac SR 75mg hai lần/ngày cùng với omeprazol 20mg một lần/ngày. Sự khác biệt có ý nghĩa về mặt lâm sàng này là do sự giảm hemoglobin (>2g/dL) và/hoặc thể tích hồng cầu (>10%) đã biết hoặc được xem là có nguồn gốc từ đường tiêu hóa. Kết quả cho từng thành phần của tiêu chí đánh giá tổng hợp này như sau:
|
Thành phần của tiêu chí đánh giá GI tổng hợp đã biết
|
Celecoxib 200mg 2 lần/ngày (N = 2238)
|
Diclofenac SR 75mg 2 lần/ngày + Omeprazol 20mg 1 lần/ngày (N = 2246)
|
|
Thành phần
|
N (%) bệnh nhân
|
|
Xuất huyết dạ dày tá tràng
|
3(0,1)
|
3(0,1)
|
|
Xuất huyết ruột già
|
1 ( < 0,1)
|
1 ( < 0,1)
|
|
Xuất huyết tiêu hóa cấp tính không rõ nguồn gốc
|
1 ( < 0,1)
|
0 (0,0)
|
|
Giảm hemoglobin (>2g/dL) và/hoặc thể tích hồng cầu (>10%) có ý nghĩa về mặt lâm sàng đã biết là có nguồn gốc GI
|
5(0,2)
|
24(1,1)
|
|
Giảm hemoglobin (>2g/dL) và/hoặc thể tích hồng cầu (>10%) có ý nghĩa về mặt lâm sàng được xem là có nguồn gốc GI
|
10 (0,4)
|
53(2,3)
|
|
Tổng*
|
20(0,9)
|
81 (3,6)
|
Đối với các thành phần sau đây của tiêu chí đánh giá GI tổng hợp đã biết, không có biến cố nào trong cả hai nhóm điều trị: tắc nghẽn lối ra của dạ dày; thủng dạ dày tá tràng, ruột non hoặc ruột già; xuất huyết ruột non. Tất cả các biến cố cấu thành tiêu chí đánh giá GI tổng hợp đã được ban giám định chuyên môn độc lập phán xét và ban giám định này không được biết đến các loại thuốc điều trị đã được cho dùng theo phương pháp ngẫu nhiên.
* Trong một phân tích tỷ lệ sống còn (time-to-event anslysis) bằng kỹ thuật bảng thống kê tuổi thọ trung bình, p < 0,0001 là xác suất dùng để so sánh giữa nhóm điều trị bằng celecoxib và nhóm điều trị bằng diclofenac kết hợp với omeprazol cho tiêu chí đánh giá này.
An toàn trên tim mạch - Nghiên cứu dài hạn trên bệnh nhân bị polyp u tuyến rải rác:
Hai nghiên cứu trên bệnh nhân bị polyp u tuyến rải rác được tiến hành với celecoxib, tức là thử nghiệm APC (Phòng ngừa u tuyến bằng Celecoxib) và thử nghiệm PreSAP (Phòng ngừa polyp u tuyến tự phát). Trong thử nghiệm APC, có sự gia tăng liên quan đến liều ở tiêu chí đánh giá tổng hợp về tử vong do tim mạch, nhồi máu cơ tim hay đột quỵ (được giám định) khi dùng celecoxib so với giả dược trong 3 năm điều trị. Thử nghiệm PreSAP không cho thấy nguy cơ gia tăng có ý nghĩa về mặt thống kê đối với tiêu chí đánh giá tổng hợp này.
Trong thử nghiệm APC, tỷ lệ nguy cơ so với giả dược ở tiêu chí đánh giá tổng hợp về tử vong do tim mạch, nhồi máu cơ tim hay đột quỵ (được giám định) là 3,4 (CI 95% 1,4 - 8,5) khi dùng celecoxib 400mg hai lần mỗi ngày và 2,8 (CI 95% 1,1 - 7,2) khi dùng celecoxib 200mg hai lần mỗi ngày. Tỉ lệ tích lũy đối với tiêu chí đánh giá tổng hợp này trong vòng 3 năm lần lượt là 3,0% (20/671) và 2,5% (17/685) đối với nhóm điều trị bằng celecoxib 200mg hai lần mỗi ngày và 400mg hai lần mỗi ngày, so với 0,9% (6/679) ở nhóm dùng giả dược. Sự gia tăng ở cả hai nhóm sử dụng celecoxib so với giả dược chủ yếu là do nhồi máu cơ tim.
Trong thử nghiệm PreSAP, tỷ lệ nguy cơ so với giả dược ở cùng tiêu chí đánh giá tổng hợp này là 1,2 (CI 95% 0,6 - 2,4) khi dùng celecoxib 400mg một lần mỗi ngày. Tỉ lệ tích lũy đối với tiêu chí đánh giá tổng hợp này qua 3 năm là 2,3% (21/933), so với 1,9% (12/628) ở nhóm dùng giả dược.
An toàn trên tim mạch - Nghiên cứu dài hạn của thử nghiệm phòng ngừa bằng thuốc kháng viêm trong bệnh Alzheimer (Nghiên cứu ADAPT)
Dữ liệu từ nghiên cứu ADAPT không cho thấy nguy cơ mắc bệnh tim mạch tăng lên đáng kể khi dùng celecoxib 200mg hai lần mỗi ngày so với giả dược. Nguy cơ tương đối so với giả dược ở một tiêu chí đánh giá tổng hợp tương tự (tử vong do tim mạch, nhồi máu cơ tim, đột quỵ) là 1,14 (CI 95% 0,61 - 2,12) khi dùng celecoxib 200mg hai lần mỗi ngày.
An toàn trên tim mạch - Phân tích tổng hợp từ các nghiên cứu về việc sử dụng thuốc lâu dài
Chưa có nghiên cứu lâm sàng có đối chứng dài hạn nào được thiết kế riêng để đánh giá sự an toàn trên tim mạch của việc dùng celecoxib lâu dài trong bất kỳ khoảng thời gian nào được tiến hành. Tuy nhiên, một phân tích tổng hợp về dữ liệu an toàn (các biến cố bất lợi nghiêm trọng do nghiên cứu viên báo cáo, đã được giám định) từ 39 nghiên cứu lâm sàng về celecoxib hoàn thành trong thời gian tối đa 65 tuần đã được tiến hành, tương ứng với 41.077 bệnh nhân [23.030 (56,1%) bệnh nhân dùng tổng liều hàng ngày (TDD) celecoxib 200mg - 800mg, 13.990 (34,1%) bệnh nhân dùng các thuốc NSAID không chọn lọc và 4.057 (9,9%) bệnh nhân dùng giả dược].
Trong phân tích này, tỷ lệ biến cố được giám định ở tiêu chí đánh giá tổng hợp (bao gồm tử vong do tim mạch, nhồi máu cơ tim không gây tử vong và đột quỵ không gây tử vong) là tương tự nhau giữa biện pháp điều trị bằng celecoxib (N = 19.773; 0,96 biến cố/100 bệnh nhân/năm) và NSAID không chọn lọc (N = 13.990; 1,12 biến cố/100 bệnh nhân/năm) (RR = 0,90, 95% CI 0,60 - 1,33). Mô hình tác dụng này được duy trì dù có dùng hay không dùng ASA ( < 325mg). Tỷ lệ biến cố được giám định là nhồi máu cơ tim không gây tử vong có xu hướng cao hơn (RR = 1,76, CI 95% 0,93 - 3,35); tuy nhiên tỷ lệ đột quỵ không gây tử vong có xu hướng thấp hơn (RR = 0,51, CI 95% 0,23 - 1,10) và tỷ lệ tử vong do tim mạch là tương đương (RR = 0,57, CI 95 % 0,28 - 1,14) khi dùng celecoxib so với dùng kết hợp các NSAID không chọn lọc.
Trong phân tích này, tỷ lệ biến cố được giám định đối với tiêu chí tổng hợp bao gồm tử vong do tim mạch, nhồi máu cơ tim không gây tử vong và đột quỵ không gây tử vong là 1,42/100 bệnh nhân/năm khi điều trị bằng celecoxib (N = 7.462) và 1,20/100 bệnh nhân/năm khi điều trị bằng giả dược (N = 4.057) (RR =1,11; CI 95% 0,47 - 2,67). Mô hình tác dụng này được duy trì dù có dùng hay không dùng ASA (< 325mg). Tỷ lệ nhồi máu cơ tim không gây tử vong có xu hướng cao hơn (RR = 1,56; CI 95% 0,21 - 11,90); tỷ lệ tử vong do bệnh tim mạch cũng cao hơn (RR = 1,26; CI 95% 0,33 - 4,77) và tỷ lệ bị đột quỵ không gây tử vong là tương tự nhau (RR = 0,80; CI 95 % 0,19 - 3,31) khi dùng celecoxib so với giả dược.
An toàn trên tim mạch
Kết quả an toàn trên tim mạch đã được đánh giá trong nghiên cứu CLASS (xem ở trên để biết mô tả của nghiên cứu). Tỷ lệ Kaplan - Meier tích lũy cho các biến cố bất lợi nghiêm trọng về huyết khối tắc nghẽn tim mạch do nghiên cứu viên báo cáo (bao gồm nhồi máu cơ tim, nghẽn mạch phổi, huyết khối tĩnh mạch sâu, đau thắt ngực không ổn định, cơn thiếu máu não thoáng qua và tai biến mạch máu não do thiếu máu cục bộ) cho thấy không có sự khác biệt giữa các nhóm điều trị bằng celecoxib, diclofenac hoặc ibuprofen. Tỷ lệ tích lũy vào thời điểm 9 tháng ở tất cả các bệnh nhân dùng celecoxib, diclofenac và ibuprofen lần lượt là 1,2%, 1,4% và 1,1%. Tỷ lệ tích lũy ở những người không sử dụng aspirin (ASA) vào thời điểm 9 tháng ở từng nhóm trong số ba nhóm điều trị đều thấp hơn 1%. Tỷ lệ tích lũy đối với nhồi máu cơ tim ở những người không dùng ASA vào thời điểm 9 tháng ở từng nhóm trong số ba nhóm điều trị đều thấp hơn 0,2%. Không có nhóm giả dược nào trong thử nghiệm CLASS, điều này giới hạn khả năng xác định xem liệu ba loại thuốc được thử nghiệm đều không có nguy cơ gia tăng biến cố tim mạch hay tất cả chúng đều làm tăng nguy cơ đến một mức độ tương tự nhau.
Các dữ liệu an toàn tiền lâm sàng
Các dữ liệu an toàn tiền lâm sàng cho thấy không có rủi ro đặc biệt nào cho con người dựa trên các nghiên cứu cơ bản về độc tính với liều nhắc lại, tác dụng gây đột biến hoặc ung thư.
Việc dùng celecoxib đường uống >150mg/kg/ngày trên thỏ đang trong quá trình tạo cơ quan (gấp xấp xỉ 2 lần so với liều sử dụng trên người 200mg hai lần/ngày tính theo AUC0-24) làm tăng tỉ lệ mắc thông liên thất, một biến cố hiếm gặp, và dị tật ở thai nhi, như là dính xương sườn, dính các đốt ức và biến dạng đốt ức. Quan sát thấy có hiện tượng tăng thoát vị cơ hoành phụ thuộc vào liều khi cho chuột cống đang trong quá trình tạo cơ quan dùng celecoxib đường uống với liều > 30mg/kg/ngày (gấp xấp xỉ 6 lần so với liều sử dụng trên người 200mg hai lần/ngày tính theo AUC0-24). Những tác động này được dự đoán xảy ra là do ức chế sự tổng hợp prostaglandin. Trên chuột cống, dùng celecoxib trong thời kỳ phát triển đầu của bào thai gây sảy thai trước và sau khi trứng làm tổ và làm giảm khả năng sống sót của phôi thai/thai nhi.
Độc tính trên động vật
Đã ghi nhận trường hợp tăng tỉ lệ bị nang tinh dịch (spermatocele) có hoặc không kèm theo những thay đổi thứ phát như giảm tinh dịch do mào tinh cũng như giãn ống dẫn tinh từ rất nhẹ đến giãn nhẹ trên chuột chưa trưởng thành. Các phát hiện trên hệ sinh sản này mặc dù có liên quan đến điều trị nhưng không làm tăng tỉ lệ hoặc mức độ nghiêm trọng theo liều dùng và có thể là tình trạng tự phát. Không ghi nhận các phát hiện tương tự trên hệ sinh sản trong nghiên cứu trên chó chưa trưởng thành, chó trưởng thành hoặc chuột trưởng thành điều trị bằng celecoxib. Chưa biết ý nghĩa lâm sàng của những quan sát này.
Đặc điểm
Viên nang cứng màu trắng đục, có 2 đai màu vàng, in số 7767 và 200.
Thông tin khác
CÁC DỮ LIỆU VỀ THỬ NGHIỆM LÂM SÀNG
Nghiên cứu lâm sàng
Thoái hoá khớp (Osteoarthritis - OA): Celecoxib đã được chứng minh có khả năng giảm đau khớp đáng kể so với giả dược. Celecoxib được đánh giá trong điều trị các dấu hiệu và triệu chứng của thoái hóa khớp gối và hông trên khoảng 4200 bệnh nhân trong thử nghiệm lâm sàng có đối chứng với giả dược và với hoạt chất khác trong thời gian tối đa 12 tuần. Ở những bệnh nhân thoái hóa khớp, điều trị bằng celecoxib 100mg hai lần mỗi ngày hoặc 200mg một lần mỗi ngày dẫn đến cải thiện được chỉ số WOMAC (Đại học Western Ontario và McMaster), là chỉ số tổng hợp các đại lượng đo lường về đau, cứng khớp và chức năng trong thoái hóa khớp. Trong ba nghiên cứu kéo dài 12 tuần về đau kèm theo bùng phát thoái hóa khớp, các liều celecoxib 100mg hai lần mỗi ngày hoặc 200mg hai lần mỗi ngày giúp giảm đau đáng kể trong vòng 24 - 48 giờ kể từ khi bắt đầu dùng thuốc. Ở mức liều 100mg hai lần mỗi ngày hoặc 200mg hai lần mỗi ngày, celecoxib đã được chứng minh có tính hiệu quả tương tự như naproxen 500mg hai lần mỗi ngày. Liều 200mg hai lần mỗi ngày không mang lại thêm lợi ích nào như đã thấy với liều 100mg hai lần mỗi ngày. Tổng liều lượng hàng ngày là 200mg đã được chứng minh là có hiệu quả như nhau cho dù dùng 100mg hai lần mỗi ngày hay 200mg một lần mỗi ngày.
Viêm khớp dạng thấp (Rheumatois arthritis - RAJ): Celecoxib đã được chứng minh có khả năng làm giảm tình trạng nhức/đau khớp và sưng khớp đáng kể so với giả dược. Celecoxib được đánh giá trong điều trị các dấu hiệu và triệu chứng của viêm khớp dạng thấp trên khoảng 2100 bệnh nhân trong thử nghiệm lâm sàng có đối chứng với giả dược và với hoạt chất khác trong thời gian tối đa 24 tuần. Celecoxib cho thấy hiệu quả vượt trội hơn giả dược trong các nghiên cứu này, bằng cách sử dụng Chỉ số đáp ứng 20 theo Hội Thấp khớp học Hoa Kỳ (American College of Rheumatology 20, ACR20), một chỉ số tổng hợp các đại lượng đo lường về lâm sàng, xét nghiệm và chức năng trong viêm khớp dạng thấp. Liều Celecoxib 100mg hai lần mỗi ngày và 200mg hai lần mỗi ngày có hiệu quả tương tự nhau và cả hai đều tương đương với naproxen 500mg hai lần mỗi ngày.
Mặc dù celecoxib 100mg hai lần mỗi ngày và 200mg hai lần mỗi ngày đều mang lại hiệu quả tổng thể tương tự nhau, nhưng một số bệnh nhân nhận được lợi ích lớn hơn từ liều 200mg hai lần mỗi ngày. Liều 400mg hai lần mỗi ngày không mang lại thêm lợi ích nào như đã thấy ở liều 100mg hay 200mg hai lần mỗi ngày.
Giảm đau, kể cả đau bụng kinh nguyên phát: Trong các mô hình giảm đau cấp tính đốii với đau sau phẫu thuật răng miệng, đau sau phẫu thuật chấn thương chỉnh hình và đau bụng kinh nguyên phát, celecoxib làm giảm cơn đau từ vừa tới nặng theo đánh giá của bệnh nhân. Liều đơn trị celecoxib giúp giảm đau trong vòng 60 phút (xem phần Liều dùng và cách dùng).
Viêm cột sống dính khớp (Ankylosing spondylitis - AS): Celecoxib đã được đánh giá ở các bệnh nhân mắc viêm cột sống dính khớp trong hai thử nghiệm lâm sàng có đối chứng với giả dược và với hoạt chất khác (naproxen hoặc ketoprofen) trong thời gian 6 và 12 tuần. Celecoxib ở các liều 100mg hai lần mỗi ngày, 200mg một lần mỗi ngày và 400mg một lần mỗi ngày đã cho thấy tác dụng vượt trội về mặt thống kê so với giả dược trong các nghiên cứu này, đối với cả ba đại lượng chính cùng đánh giá tính hiệu quả bao gồm: đánh giá mức độ đau tổng thể (Thang điểm ước lượng trực quan), mức độ hoạt động tổng thể của bệnh (Thang điểm ước lượng trực quan) và suy giảm chức năng (Chỉ số chức năng viêm cột sống dính khớp Bath). Trong nghiên cứu kéo dài 12 tuần, không có sự khác biệt về mức độ cải thiện giữa liều 200mg và 400mg celecoxib khi so sánh mức độ thay đổi trung bình so với ban đầu, nhưng tỷ lệ bệnh nhân đáp ứng với celecoxib 400mg là 53%, lớn hơn so với celecoxib 200mg, là 44%, bằng phương pháp Đánh giá dựa trên tiêu chí đáp ứng trong viêm cột sống dính khớp (ASAS 20). ASAS 20 định nghĩa người đáp ứng là người đạt mức độ cải thiện so với ban đầu ít nhất 20% và mức độ cải thiện tuyệt đối ít nhất là 10mm, trên thang điểm từ 0 đến 100mm, ở ít nhất ba trong tổng sổ bốn yếu tố sau: đánh giá tổng thể bệnh nhân, đau, chỉ số chức năng viêm cột sống dính khớp Bath và viêm. Phân tích đáp ứng cũng cho thấy không có sự thay đổi nào về tỷ lệ đáp ứng khi vượt quá 6 tuần.
Thông tin thêm từ nghiên cứu lâm sàng
Nghiên cứu nội soi
Đánh giá nội soi đường tiêu hóa trên theo định kỳ được thực hiện trên hơn 4.500 bệnh nhân viêm khớp tham gia trong 5 thử nghiệm ngẫu nhiên có đối chứng kéo dài 12 - 24 tuần đối chứng với hoạt chất khác, 2 trong số các nghiên cứu này cũng có đối chứng bằng giả dược. Không có mối quan hệ nhất quán nào giữa tỷ lệ mắc viêm loét dạ dày tá tràng với liều celecoxib trong phạm vi nghiên cứu.
Bảng 3 tóm tắt tỷ lệ loét qua nội soi trong hai nghiên cứu 12 tuần trong đó bệnh nhân tham gia có kết quả nội soi ban đầu không phát hiện vết loét nào.
Bảng 3. Tỉ lệ loét dạ dày tá tràng từ các nghiên cứu nội soi ở bệnh nhân thoái hóa khớp và viêm khớp dạng thấp
| |
Nghiên cứu 3 tháng
|
| |
Nghiên cứu 1 (N = 1108)
|
Nghiên cứu 2 (N= 1049)
|
|
Giả dược
|
2,3% (5/217)
|
2,0% (4/200)
|
|
Celecoxib 50mg, 2 lần/ngày
|
3,4% (8/233)
|
...
|
|
Celecoxib 100mg, 2 lần/ngày
|
3,1% (7/227)
|
4,0% (9/223)
|
|
Celecoxib 200mg, 2 lần/ngày
|
5,9% (13/221)
|
2,7% (6/219)
|
|
Celecoxib 400mg, 2 lần/ngày
|
...
|
4,1% (8/197)
|
|
Naproxen 500mg, 2 lần/ngày
|
16,2% (34/210)*
|
17,6% (37/210)*
|
* p ≤ 0,05 so với tất cả các phương pháp điều trị khác.
Bảng 4 tóm tắt dữ liệu từ hai nghiên cứu 12 tuần trong đó bệnh nhân tham gia có kết quả nội soi ban đầu không phát hiện vết loét nào. Bệnh nhân đã thực hiện nội soi theo định kỳ 4 tuần một lần để cung cấp thông tin về nguy cơ loét theo thời gian.
Bảng 4. Tỉ lệ loét dạ dày tá tràng từ các nghiên cứu nội soi liên tiếp trong 3 tháng ở bệnh nhân thoái hóa khớp và viêm khớp dạng thấp
| |
Tuần 4
|
Tuần 8
|
Tuần 12
|
Tuần cuối cùng
|
|
Nghiên cứu 3 (N=523)
|
|
Celecoxib
|
4.0%
|
2.2%
|
1.5%
|
7.5%
|
|
200mg 2 lần/ngày
|
(10/252)*
|
(5/227)*
|
(3/196)*
|
(20/266)*
|
|
Naproxen
|
19.0%
|
14.2%
|
9.9%
|
34.6%
|
|
500mg 2 lần/ngày
|
(47/247)
|
(26/182)
|
(14/141)
|
(89/257)
|
|
Nghiên cứu 4 (N = 1062)
|
|
Celecoxib
|
3.9%
|
2.4%
|
1.8%
|
7.0%
|
|
200mg 2 lần/ngày
|
(13/337)+
|
(7/296) +
|
(5/274)+
|
(25/356)+
|
|
Diclofenac
|
5.1%
|
3.3%
|
2.9%
|
9.7%
|
|
75mg 2 lần/ngày
|
(18/350)
|
(10/306)
|
(8/278)
|
(36/372)
|
|
Ibuprofen
|
13.0%
|
6.2%
|
9.6%
|
23.3%
|
|
800mg 3 lần/ngày
|
(42/323)
|
(15/241)
|
(21/219)
|
(78/334)
|
*p ≤ 0,05 celecoxib so với naproxen dựa trên các phân tích theo định kì và tích lũy
+p ≤ 0,05 celecoxib so với ibuprofen dựa trên các phân tích theo định kỳ và tích lũy.
Một nghiên cứu ngẫu nhiên và mù đôi kéo dài 6 tháng trên 430 bệnh nhân viêm khớp dạng thấp đã được tiến hành, trong đó đã thực hiện kiểm tra nội soi vào thời điểm 6 tháng.
Tỷ lệ loét qua nội soi ở bệnh nhân dùng celecoxib 200mg hai lần mỗi ngày là 4%, so với 15% ở bệnh nhân dùng diclofenac SR 75mg hai lần mỗi ngày (p < 0,001).
Trong số 4 trên 5 nghiên cứu nội soi, khoảng 11% bệnh nhân (440/4000) có dùng aspirin (≤ 325mg/ngày). Ở nhóm dùng celecoxib, tỷ lệ loét qua nội soi ở những người sử dụng aspirin cao hơn so với người không sử dụng. Tuy nhiên, tỷ lệ gia tăng loét ở những người sử dụng aspirin thấp hơn so với tỷ lệ loét qua nội soi quan sát thấy ở các nhóm dùng hoạt chất so sánh, có dùng hoặc không dùng aspirin.
Chưa xác lập được mối tương quan nào giữa kết quả của nghiên cứu nội soi và tỷ lệ tương đối của các biến cố nghiêm trọng có ý nghĩa về mặt lâm sàng ở đường tiêu hoá trên. Xuất huyết đường tiêu hóa trên nghiêm trọng có ý nghĩa về mặt lâm sàng đã được quan sát thấy ở những bệnh nhân dùng celecoxib trong các thử nghiệm có đối chứng và nhãn mở, mặc dù không thường xuyên (xem phần Các tác động trên đường tiêu hóa)
Phân tích tổng hợp về tính an toàn trên đường tiêu hóa từ các nghiên cứu thoái hoá khớp và viêm khớp dạng thấp
Một phân tích dựa trên 31 nghiên cứu lâm sàng ngẫu nhiên có đối chứng về thoái hoá khớp và viêm khớp dạng thấp, bao gồm 39.605 bệnh nhân thoái hoá khớp (N = 25.903), viêm khớp dạng thấp (N = 3.232) hoặc những bệnh nhân mắc một trong hai tình trạng này (N = 10.470), và so sánh tỷ lệ mắc các tác dụng không mong muốn trên đường tiêu hoá ở bệnh nhân được điều trị bằng celecoxib với bệnh nhân dùng giả dược hoặc các NSAID khác (bao gồm cả naproxen, diclofenac và ibuprofen). Tỷ lệ loét trên lâm sàng và xuất huyết do loét khi dùng tổng liều hàng ngày celecoxib 200mg - 400mg là 0,2%, so với tỉ lệ 0,6% khi dùng các NSAID khác (RR = 0,35; CI 95% 0,22 - 0,56).
Nghiên cứu tính an toàn lâu dài của celecoxib trong điều trị Viêm xương khớp (nghiên cứu CLASS) bao gồm cả việc sử dụng cùng với aspirin
Trong một nghiên cứu tiên cứu về kết quả an toàn dài hạn được tiến hành sau khi đưa thuốc ra thị trường ở khoảng 5.800 bệnh nhân mắc bệnh thoái hóa khớp và 2.200 bệnh nhân mắc bệnh viêm khớp dạng thấp, bệnh nhân đã dùng celecoxib 400mg hai lần mỗi ngày (lần lượt gấp 4 lần và gấp 2 lần liều khuyến cáo dùng cho thoái hóa khớp và viêm khớp dạng thấp), ibuprofen 800mg ba lần mỗi ngày hoặc diclofenac 75mg hai lần mỗi ngày (liều điều trị thông thường). Thời gian sử dụng trung bình với celecoxib (N = 3.987) và diclofenac (N = 1.996) là 9 tháng trong khi ibuprofen (N = 1.985) là 6 tháng. Tỷ lệ Kaplan-Meier tích lũy vào thời điểm 9 tháng được cung cấp cho tất cả các phân tích. Tiêu chí đánh giá chính của kết quả nghiên cứu này là tỷ lệ viêm loét có biến chứng (xuất huyết, thủng hoặc tắc nghẽn đường tiêu hóa). Bệnh nhân được phép dùng đồng thời aspirin (ASA) liều thấp (< 325mg/ngày) để phòng bệnh tim mạch (phân nhóm ASA: celecoxib, N = 882; diclofenac, N = 445; ibuprofen, N = 412). Sự khác biệt về tỷ lệ viêm loét có biến chứng giữa celecoxib và nhóm dùng kết hợp ibuprofen và diclofenac không có ý nghĩa về mặt thống kê. Những bệnh nhân dùng đồng thời celecoxib và ASA liều thấp có tỉ lệ viêm loét có biến chứng cao gấp 4 lần so với bệnh nhân không dùng ASA (xem phần Các tác động trên đường tiêu hóa).
Các kết quả về celecoxib được trình bày trong Bảng 5.
Bảng 5. Ảnh hưởng của việc dùng đồng thời Aspirin liều thấp lên tỷ lệ loét có biến chứng với Celecoxib 400mg 2 lần/ngày (tỷ lệ Kaplan-Meier ở 9 tháng [%])
| |
Người không dùng aspirin N = 3105
|
Người dùng aspirin N = 882
|
|
Loét có biến chứng
|
0,32
|
1,12
|
Chức năng tiểu cầu
Trên người tình nguyện khỏe mạnh, celecoxib ở các mức liều điều trị và ở các mức đa liều 600mg hai lần mỗi ngày (gấp ba lần so với liều khuyến cáo cao nhất) không gây ảnh hưởng trên quá trình kết tập tiểu cầu và thời gian xuất huyết khi so sánh với giả dược. Tất cả các nhóm đối chứng với hoạt chất khác (chất ức chế COX không đặc hiệu) đều thấy giảm đáng kể khả năng kết tập tiểu cầu và kéo dài thời gian xuất huyết (xem Hình 1). Nghiên cứu so sánh celecoxib với omeprazol và diclofenac trên những bệnh nhân có nguy cơ mắc thoái hoá khớp và viêm khớp dạng thấp (Nghiên cứu CONDOR)
Nghiên cứu so sánh celecoxib với omeprazol và diclofenac trên những bệnh nhân có nguy cơ mắc thoái hoá khớp và viêm khớp dạng thấp (Nghiên cứu CONDOR)
Trong nghiên cứu tiến cứu kéo dài 24 tuần ở bệnh nhân > 60 tuổi hoặc có tiền sử loét dạ dày tá tràng (trừ người sử dụng aspirin liều thấp), tỷ lệ phần trăm bệnh nhân gặp các biến cố về tiêu hóa (GI) có ý nghĩa về mặt lâm sàng (tiêu chí đánh giá tổng hợp chính) thấp hơn ở những bệnh nhân được điều trị bằng celecoxib 200mg hai lần/ngày so với những bệnh nhân được điều trị bằng diclofenac SR 75mg hai lần/ngày cùng với omeprazol 20mg một lần/ngày. Sự khác biệt có ý nghĩa về mặt lâm sàng này là do sự giảm hemoglobin (>2g/dL) và/hoặc thể tích hồng cầu (>10%) đã biết hoặc được xem là có nguồn gốc từ đường tiêu hóa. Kết quả cho từng thành phần của tiêu chí đánh giá tổng hợp này như sau:
|
Thành phần của tiêu chí đánh giá GI tổng hợp đã biết
|
Celecoxib 200mg 2 lần/ngày (N = 2238)
|
Diclofenac SR 75mg 2 lần/ngày + Omeprazol 20mg 1 lần/ngày (N = 2246)
|
|
Thành phần
|
N (%) bệnh nhân
|
|
Xuất huyết dạ dày tá tràng
|
3(0,1)
|
3(0,1)
|
|
Xuất huyết ruột già
|
1 ( < 0,1)
|
1 ( < 0,1)
|
|
Xuất huyết tiêu hóa cấp tính không rõ nguồn gốc
|
1 ( < 0,1)
|
0 (0,0)
|
|
Giảm hemoglobin (>2g/dL) và/hoặc thể tích hồng cầu (>10%) có ý nghĩa về mặt lâm sàng đã biết là có nguồn gốc GI
|
5(0,2)
|
24(1,1)
|
|
Giảm hemoglobin (>2g/dL) và/hoặc thể tích hồng cầu (>10%) có ý nghĩa về mặt lâm sàng được xem là có nguồn gốc GI
|
10 (0,4)
|
53(2,3)
|
|
Tổng*
|
20(0,9)
|
81 (3,6)
|
Đối với các thành phần sau đây của tiêu chí đánh giá GI tổng hợp đã biết, không có biến cố nào trong cả hai nhóm điều trị: tắc nghẽn lối ra của dạ dày; thủng dạ dày tá tràng, ruột non hoặc ruột già; xuất huyết ruột non. Tất cả các biến cố cấu thành tiêu chí đánh giá GI tổng hợp đã được ban giám định chuyên môn độc lập phán xét và ban giám định này không được biết đến các loại thuốc điều trị đã được cho dùng theo phương pháp ngẫu nhiên.
* Trong một phân tích tỷ lệ sống còn (time-to-event anslysis) bằng kỹ thuật bảng thống kê tuổi thọ trung bình, p < 0,0001 là xác suất dùng để so sánh giữa nhóm điều trị bằng celecoxib và nhóm điều trị bằng diclofenac kết hợp với omeprazol cho tiêu chí đánh giá này.
An toàn trên tim mạch - Nghiên cứu dài hạn trên bệnh nhân bị polyp u tuyến rải rác:
Hai nghiên cứu trên bệnh nhân bị polyp u tuyến rải rác được tiến hành với celecoxib, tức là thử nghiệm APC (Phòng ngừa u tuyến bằng Celecoxib) và thử nghiệm PreSAP (Phòng ngừa polyp u tuyến tự phát). Trong thử nghiệm APC, có sự gia tăng liên quan đến liều ở tiêu chí đánh giá tổng hợp về tử vong do tim mạch, nhồi máu cơ tim hay đột quỵ (được giám định) khi dùng celecoxib so với giả dược trong 3 năm điều trị. Thử nghiệm PreSAP không cho thấy nguy cơ gia tăng có ý nghĩa về mặt thống kê đối với tiêu chí đánh giá tổng hợp này.
Trong thử nghiệm APC, tỷ lệ nguy cơ so với giả dược ở tiêu chí đánh giá tổng hợp về tử vong do tim mạch, nhồi máu cơ tim hay đột quỵ (được giám định) là 3,4 (CI 95% 1,4 - 8,5) khi dùng celecoxib 400mg hai lần mỗi ngày và 2,8 (CI 95% 1,1 - 7,2) khi dùng celecoxib 200mg hai lần mỗi ngày. Tỉ lệ tích lũy đối với tiêu chí đánh giá tổng hợp này trong vòng 3 năm lần lượt là 3,0% (20/671) và 2,5% (17/685) đối với nhóm điều trị bằng celecoxib 200mg hai lần mỗi ngày và 400mg hai lần mỗi ngày, so với 0,9% (6/679) ở nhóm dùng giả dược. Sự gia tăng ở cả hai nhóm sử dụng celecoxib so với giả dược chủ yếu là do nhồi máu cơ tim.
Trong thử nghiệm PreSAP, tỷ lệ nguy cơ so với giả dược ở cùng tiêu chí đánh giá tổng hợp này là 1,2 (CI 95% 0,6 - 2,4) khi dùng celecoxib 400mg một lần mỗi ngày. Tỉ lệ tích lũy đối với tiêu chí đánh giá tổng hợp này qua 3 năm là 2,3% (21/933), so với 1,9% (12/628) ở nhóm dùng giả dược.
An toàn trên tim mạch - Nghiên cứu dài hạn của thử nghiệm phòng ngừa bằng thuốc kháng viêm trong bệnh Alzheimer (Nghiên cứu ADAPT)
Dữ liệu từ nghiên cứu ADAPT không cho thấy nguy cơ mắc bệnh tim mạch tăng lên đáng kể khi dùng celecoxib 200mg hai lần mỗi ngày so với giả dược. Nguy cơ tương đối so với giả dược ở một tiêu chí đánh giá tổng hợp tương tự (tử vong do tim mạch, nhồi máu cơ tim, đột quỵ) là 1,14 (CI 95% 0,61 - 2,12) khi dùng celecoxib 200mg hai lần mỗi ngày.
An toàn trên tim mạch - Phân tích tổng hợp từ các nghiên cứu về việc sử dụng thuốc lâu dài
Chưa có nghiên cứu lâm sàng có đối chứng dài hạn nào được thiết kế riêng để đánh giá sự an toàn trên tim mạch của việc dùng celecoxib lâu dài trong bất kỳ khoảng thời gian nào được tiến hành. Tuy nhiên, một phân tích tổng hợp về dữ liệu an toàn (các biến cố bất lợi nghiêm trọng do nghiên cứu viên báo cáo, đã được giám định) từ 39 nghiên cứu lâm sàng về celecoxib hoàn thành trong thời gian tối đa 65 tuần đã được tiến hành, tương ứng với 41.077 bệnh nhân [23.030 (56,1%) bệnh nhân dùng tổng liều hàng ngày (TDD) celecoxib 200mg - 800mg, 13.990 (34,1%) bệnh nhân dùng các thuốc NSAID không chọn lọc và 4.057 (9,9%) bệnh nhân dùng giả dược].
Trong phân tích này, tỷ lệ biến cố được giám định ở tiêu chí đánh giá tổng hợp (bao gồm tử vong do tim mạch, nhồi máu cơ tim không gây tử vong và đột quỵ không gây tử vong) là tương tự nhau giữa biện pháp điều trị bằng celecoxib (N = 19.773; 0,96 biến cố/100 bệnh nhân/năm) và NSAID không chọn lọc (N = 13.990; 1,12 biến cố/100 bệnh nhân/năm) (RR = 0,90, 95% CI 0,60 - 1,33). Mô hình tác dụng này được duy trì dù có dùng hay không dùng ASA ( < 325mg). Tỷ lệ biến cố được giám định là nhồi máu cơ tim không gây tử vong có xu hướng cao hơn (RR = 1,76, CI 95% 0,93 - 3,35); tuy nhiên tỷ lệ đột quỵ không gây tử vong có xu hướng thấp hơn (RR = 0,51, CI 95% 0,23 - 1,10) và tỷ lệ tử vong do tim mạch là tương đương (RR = 0,57, CI 95 % 0,28 - 1,14) khi dùng celecoxib so với dùng kết hợp các NSAID không chọn lọc.
Trong phân tích này, tỷ lệ biến cố được giám định đối với tiêu chí tổng hợp bao gồm tử vong do tim mạch, nhồi máu cơ tim không gây tử vong và đột quỵ không gây tử vong là 1,42/100 bệnh nhân/năm khi điều trị bằng celecoxib (N = 7.462) và 1,20/100 bệnh nhân/năm khi điều trị bằng giả dược (N = 4.057) (RR =1,11; CI 95% 0,47 - 2,67). Mô hình tác dụng này được duy trì dù có dùng hay không dùng ASA (< 325mg). Tỷ lệ nhồi máu cơ tim không gây tử vong có xu hướng cao hơn (RR = 1,56; CI 95% 0,21 - 11,90); tỷ lệ tử vong do bệnh tim mạch cũng cao hơn (RR = 1,26; CI 95% 0,33 - 4,77) và tỷ lệ bị đột quỵ không gây tử vong là tương tự nhau (RR = 0,80; CI 95 % 0,19 - 3,31) khi dùng celecoxib so với giả dược.
An toàn trên tim mạch
Kết quả an toàn trên tim mạch đã được đánh giá trong nghiên cứu CLASS (xem ở trên để biết mô tả của nghiên cứu). Tỷ lệ Kaplan - Meier tích lũy cho các biến cố bất lợi nghiêm trọng về huyết khối tắc nghẽn tim mạch do nghiên cứu viên báo cáo (bao gồm nhồi máu cơ tim, nghẽn mạch phổi, huyết khối tĩnh mạch sâu, đau thắt ngực không ổn định, cơn thiếu máu não thoáng qua và tai biến mạch máu não do thiếu máu cục bộ) cho thấy không có sự khác biệt giữa các nhóm điều trị bằng celecoxib, diclofenac hoặc ibuprofen. Tỷ lệ tích lũy vào thời điểm 9 tháng ở tất cả các bệnh nhân dùng celecoxib, diclofenac và ibuprofen lần lượt là 1,2%, 1,4% và 1,1%. Tỷ lệ tích lũy ở những người không sử dụng aspirin (ASA) vào thời điểm 9 tháng ở từng nhóm trong số ba nhóm điều trị đều thấp hơn 1%. Tỷ lệ tích lũy đối với nhồi máu cơ tim ở những người không dùng ASA vào thời điểm 9 tháng ở từng nhóm trong số ba nhóm điều trị đều thấp hơn 0,2%. Không có nhóm giả dược nào trong thử nghiệm CLASS, điều này giới hạn khả năng xác định xem liệu ba loại thuốc được thử nghiệm đều không có nguy cơ gia tăng biến cố tim mạch hay tất cả chúng đều làm tăng nguy cơ đến một mức độ tương tự nhau.
Các dữ liệu an toàn tiền lâm sàng
Các dữ liệu an toàn tiền lâm sàng cho thấy không có rủi ro đặc biệt nào cho con người dựa trên các nghiên cứu cơ bản về độc tính với liều nhắc lại, tác dụng gây đột biến hoặc ung thư.
Việc dùng celecoxib đường uống >150mg/kg/ngày trên thỏ đang trong quá trình tạo cơ quan (gấp xấp xỉ 2 lần so với liều sử dụng trên người 200mg hai lần/ngày tính theo AUC0-24) làm tăng tỉ lệ mắc thông liên thất, một biến cố hiếm gặp, và dị tật ở thai nhi, như là dính xương sườn, dính các đốt ức và biến dạng đốt ức. Quan sát thấy có hiện tượng tăng thoát vị cơ hoành phụ thuộc vào liều khi cho chuột cống đang trong quá trình tạo cơ quan dùng celecoxib đường uống với liều > 30mg/kg/ngày (gấp xấp xỉ 6 lần so với liều sử dụng trên người 200mg hai lần/ngày tính theo AUC0-24). Những tác động này được dự đoán xảy ra là do ức chế sự tổng hợp prostaglandin. Trên chuột cống, dùng celecoxib trong thời kỳ phát triển đầu của bào thai gây sảy thai trước và sau khi trứng làm tổ và làm giảm khả năng sống sót của phôi thai/thai nhi.
Độc tính trên động vật
Đã ghi nhận trường hợp tăng tỉ lệ bị nang tinh dịch (spermatocele) có hoặc không kèm theo những thay đổi thứ phát như giảm tinh dịch do mào tinh cũng như giãn ống dẫn tinh từ rất nhẹ đến giãn nhẹ trên chuột chưa trưởng thành. Các phát hiện trên hệ sinh sản này mặc dù có liên quan đến điều trị nhưng không làm tăng tỉ lệ hoặc mức độ nghiêm trọng theo liều dùng và có thể là tình trạng tự phát. Không ghi nhận các phát hiện tương tự trên hệ sinh sản trong nghiên cứu trên chó chưa trưởng thành, chó trưởng thành hoặc chuột trưởng thành điều trị bằng celecoxib. Chưa biết ý nghĩa lâm sàng của những quan sát này.