Lưu ý khi sử dụng (Cảnh báo và thận trọng)
Cảnh báo chung
Không nên sử dụng SPIOLTO RESPIMAT nhiều hơn 1 lần mỗi ngày.
Không nên sử dụng SPIOLTO RESPIMAT trên bệnh nhân hen. Độ an toàn và hiệu lực của SPIOLTO RESPIMAT trên bệnh nhân hen chưa được nghiên cứu.
Co thắt phế quản cấp
SPIOLTO RESPIMAT không được chỉ định để điều trị cơn co thắt phế quản cấp, nghĩa là không được sử dụng làm thuốc cắt cơn.
Quá mẫn
Tương tự tất cả các thuốc khác, phản ứng quá mẫn có thể xuất hiện ngay sau khi sử dụng SPIOLTO RESPIMAT.
Co thắt phế quản nghịch thường
Tương tự như các thuốc dạng hít khác, SPIOLTO RESPIMAT có thể gây co thắt phế quản nghịch thường đe dọa tính mạng. Nếu xuất hiện co thắt phế quản nghịch thường, nên ngừng thuốc ngay lập tức và sử dụng liệu pháp thay thế.
Tăng nhãn áp góc hẹp, tăng sinh tuyến tiền liệt hoặc tắc nghẽn cổ bàng quang
Do đặc tính kháng cholinergic của tiotropium, cần sử dụng thận trọng SPIOLTO RESPIMAT trên bệnh nhân tăng nhãn áp góc đóng, tăng sinh tuyến tiền liệt, hoặc tắc nghẽn cổ bàng quang.
Bệnh nhân suy thận
Do nồng độ trong huyết tương của tiotropiumm tăng lên khi chức năng thận giảm ở bệnh nhân suy thận trung bình đến nặng (độ thanh thải creatinine ≤ 50mL/phút), chỉ nên dùng Spiolto Respimat khi lợi ích mong đợi vượt trội nguy cơ có thể xảy ra.
Chưa có kinh nghiệm sử dụng thuốc lâu dài trên bệnh nhân suy thận nặng (xem mục Đặc điểm dược động học).
Triệu chứng trên mắt
Bệnh nhân phải được hướng dẫn sử dụng SPIOLTO RESPIMAT đúng cách. Phải thận trọng, không được để dung dịch hoặc khí dung hạt mịn bay vào mắt. Đau mắt hoặc cảm giác khó chịu, nhìn mờ, nhìn quầng sáng hoặc hình ảnh có nhiều màu sắc kèm theo mắt đỏ do sung huyết kết mạc và phù nề giác mạc có thể là dấu hiệu của tăng nhãn áp góc hẹp cấp. Nên khám chuyên khoa ngay nếu xuất hiện bất kỳ sự kết hợp nào của các triệu chứng nêu trên.
Các thuốc nhỏ mắt gây co đồng tử không được cân nhắc trong điều trị các triệu chứng trên.
Ảnh hưởng trên tim mạch
SPIOLTO RESPIMAT chứa một chất chủ vận beta2-adrenergic tác dụng kéo dài. Các chất chủ vận beta2-adrenergic tác dụng kéo dài nên được sử dụng thận trọng trên bệnh nhân mắc bệnh tim mạch, đặc biệt là suy mạch vành, loạn nhịp tim, bệnh cơ tim phì đại tắc nghẽn và tăng huyết áp; trên bệnh nhân mắc chứng co giật hoặc nhiễm độc giáp, bệnh nhân có tiền sử hoặc nghi ngờ có khoảng QT kéo dài, bệnh nhân có đáp ứng bất thường với các amin cường giao cảm.
Tương tự các chất chủ vận beta2-adrenergic khác, olodaterol có thể ảnh hưởng trên tim mạch có ý nghĩa lâm sàng ở một số bệnh nhân, biểu hiện bằng tăng nhịp tim, tăng huyết áp và/hoặc các triệu chứng lâm sàng. Có thể cần ngừng sử dụng thuốc khi ảnh hưởng này xuất hiện. Hơn nữa, các thuốc chủ vận beta2-adrenergic đã được ghi nhận là nguyên nhân gây ra những thay đổi trên điện tâm đồ (ECG), như làm dẹt sóng T và đoạn ST chênh xuống, mặc dù ý nghĩa lâm sàng của những ghi nhận này chưa rõ ràng.
Hạ kali huyết
Các thuốc chủ vận beta2-adrenergic có thể gây hạ kali huyết đáng kể trên một số bệnh nhân, và có khả năng dẫn đến những tác dụng bất lợi trên tim mạch. Giảm nồng độ kali huyết thanh thường thoáng qua và không yêu cầu bổ sung kali. Bệnh nhân COPD nặng có khả năng hạ kali huyết do tình trạng thiếu oxy và các điều trị kèm theo (xem phần Tương tác), dẫn đến tăng nhạy cảm với loạn nhịp tim.
Tăng đường huyết
Các thuốc chủ vận beta2-adrenergic dạng hít liều cao có thể gây tăng nồng độ đường huyết tương.
Khi dùng cùng các thuốc gây mê
Cần thận trọng trong trường hợp có kế hoạch phẫu thuật sử dụng thuốc gây mê hydrocarbon halogen hoá do sự tăng nhạy cảm với các tác dụng phụ trên tim mạch của các thuốc giãn phế quản chủ vận beta.
Không nên sử dụng SPIOLTO RESPIMAT đồng thời với các thuốc khác chứa chất chủ vận beta2-adrenergic tác dụng kéo dài. Những bệnh nhân đang sử dụng thường xuyên các chất chủ vận beta2-adrenergic tác dụng ngắn dạng hít (ví dụ 4 lần/ngày) cần được khuyến cáo chỉ sử dụng các tác nhân này để làm giảm các triệu chứng hô hấp cấp.
Tác dụng không mong muốn (Tác dụng phụ)
Độ an toàn của SPIOLTO RESPIMAT được đánh giá qua các thử nghiệm lâm sàng bắt chéo, nhóm song song và đối chứng với chất hoạt tính trên 7151 bệnh nhân COPD. Tổng cộng có 1988 bệnh nhân COPD sử dụng mức liều mục tiêu là 5 microgram tiotropium và 5 microgram olodaterol.
Các tác dụng không mong muốn của SPIOLTO RESPIMAT được xác định chủ yếu dựa trên các dữ liệu thu được từ 2 thử nghiệm lâm sàng nhóm song song, đối chứng với chất hoạt tính, điều trị kéo dài (52 tuần) trên bệnh nhân COPD.
Trong phân tích gộp hai thử nghiệm lâm sàng điều trị kéo dài này, tỷ lệ chung của các biến cố bất lợi trên nhóm bệnh nhân sử dụng SPIOLTO RESPIMAT tương đương với nhóm bệnh nhân sử dụng đơn độc tiotropium liều 5 microgram hoặc olodaterol liều 5 microgram (lần lượt là 74%, 73,3% và 76,6%).
Bất kỳ các tác dụng không mong muốn nào được ghi nhận trước đây đối với một trong hai thành phần của thuốc cũng được coi là tác dụng ngoại ý của SPIOLTO RESPIMAT và được liệt kê trong danh sách dưới đây.
Ngoài ra, danh sách này cũng gồm các tác dụng ngoại ý được ghi nhận đối với SPIOLTO RESPIMAT nhưng chưa được ghi nhận khi sử dụng đơn độc từng thành phần.
Nhiễm khuẩn và ký sinh trùng: Viêm mũi họng
Rối loạn chuyển hóa và dinh dưỡng: Mất nước
Rối loạn hệ thần kinh: Chóng mặt, mất ngủ
Rối loạn trên mắt: Tăng nhãn áp, tăng áp lực nội nhãn, nhìn mờ
Rối loạn trên tim: Rung nhĩ, đánh trống ngực, nhịp nhanh trên thất. nhịp tim nhanh
Rối loạn hệ mạch: Tăng huyết áp
Rối loạn hô hấp, lồng ngực và trung thất: Ho, chảy máu cam, viêm họng, khó phát âm, co thắt phế quản, viêm thanh quản, viêm xoang
Rối loạn tiêu hóa: Khô miệng, thường nhẹ; táo bón; nhiễm nấm Candida hầu họng; khó nuốt; trào ngược dạ dày thực quản; viêm lợi; viêm lưỡi; việm miệng; tắc ruột bao gồm liệt ruột
Rối loạn trên da và mô dưới da: Phát ban, ngứa, phù mạch thần kinh, mề đay, nhiễm trùng da và loét da, khô da, quá mẫn (gồm các phản ứng quá mẫn tức thì)
Rối loạn cơ xương khớp và mô liên kết: Đau khớp, sưng khớp, đau lưng1 (1các tác dụng ngoại ý ghi nhận với SPIOLTO RESPIMAT nhưng không được ghi nhận với từng thành phần).
Rối loạn thận và tiết niệu: Bí tiểu (thường gặp ở nam giới có yếu tố nguy cơ), tiểu khó, nhiễm trùng đường niệu
Nhiều tác dụng không mong muốn đã được liệt kê ở trên có thể do hoạt tính kháng cholinergic của tiotropium hoặc do hoạt tính beta-adrenergic của olodaterol - hai thành phần của SPIOLTO RESPIMAT.
Ngoài ra, cũng cần lưu ý các tác dụng ngoại ý khác liên quan đến các chất chủ vận beta-adrenergic chưa được liệt kê ở trên như loạn nhịp, thiếu máu cơ tim, đau thắt ngực, hạ huyết áp, run, đau đầu, căng thẳng, buồn nôn, co thắt cơ, mệt mỏi, khó chịu, hạ kali huyết, tăng đường huyết và toan chuyển hóa.
Dược lý
Nhóm dược lý điều trị: Thuốc điều trị bệnh lý tắc nghẽn đường hô hấp, thuốc chủ vận adrenergic phối hợp với thuốc kháng cholinergic.
Mã ATC: RO3ALxx
Cơ chế tác dụng
Tiotropium, một thuốc kháng muscarinic tác dụng kéo dài, và olodaterol, một thuốc chủ vận beta2-adrenergic tác dụng kéo dài, được phối hợp trong bình xịt hạt mịn SPIOLTO RESPIMAT. Hai hoạt chất này hiệp đồng tác dụng giãn phế quản do chúng có cơ chế tác dụng khác nhau và vị trí đích tác dụng trên phổi khác nhau.
Tiotropium
Tiotropium bromide là thuốc đối kháng thụ thể muscarinic tác dụng kéo dài (LAMA), trên lâm sàng thường gọi là kháng cholinergic. Thuốc có ái lực tương đương trên các thụ thể muscarinic từ M1 đến M5. Trên đường dẫn khí, thuốc ức chế thụ thể M3 trên cơ trơn gây giãn cơ. Tính đối kháng cạnh tranh và thuận nghịch đã được thể hiện trên các thụ thể ở người, động vật và các cơ quan phân lập. Trong các nghiên cứu tiền lâm sàng in vitro cũng như in vivo, tác dụng bảo vệ phế quản phụ thuộc vào liều và kéo dài trên 24 giờ. Thời gian tác dụng kéo dài có thể do tốc độ phân ly rất chậm của thuốc từ thụ thể M3, thể hiện ở thời gian bán phân ly dài hơn đáng kể so với ipratropium. Tương tự các thuốc kháng cholinergic chứa nhóm N bậc IV, tiotropium có tác dụng chọn lọc tại chỗ (phế quản) khi được dùng dạng hít, do đó thuốc có khoảng điều trị chấp nhận được trước khi tác dụng kháng cholinergic toàn thân tăng lên. Tốc độ phân ly từ thụ thể M2 nhanh hơn từ thụ thể M3, điều này giải thích tính chọn lọc của thuốc trên thụ thể M3 so với M2 trong các nghiên cứu chức năng in vitro (có kiểm soát động học).
Tiềm lực gắn cao và tốc độ phân li từ thụ thể chậm có mối tương quan về mặt lâm sàng, thể hiện ở tác dụng giãn phế quản đáng kể và kéo dài trên bệnh nhân COPD.
Tác dụng giãn phế quản sau khi hít tiotropium chủ yếu do tác dụng tại chỗ (trên đường dẫn khí), không phải do tác dụng toàn thân của thuốc này.
Olodaterol
Olodaterol có ái lực mạnh và tính chọn lọc cao đối với thụ thể beta2-adrenergic của người. Các nghiên cứu in vitro cho thấy olodaterol có tính chủ vận trên thụ thể beta2-adrenergic mạnh hơn 241 lần so với thụ thể beta1-adrenergic và mạnh hơn 2299 lần so với thụ thể beta3-adrenergic. Tác dụng dược lý của chất này được tạo ra nhờ khả năng liên kết và hoạt hóa thụ thể beta2-adrenergic sau khi dùng tại chỗ theo đường hít.
Hoạt hóa các thụ thể này trên đường dẫn khí gây kích thích adenyl cyclase nội sinh, một enzym trung gian trong quá trình tổng hợp 3’,5’-adenosine monophosphate vòng (cAMP). Tăng nồng độ cAMP gây giãn phế quản thông qua giãn các tế bào cơ trơn đường dẫn khí. Olodaterol có đặc tính tiền lâm sàng của chất chủ vận chọn lọc thụ thể beta2-adrenergic tác dụng kéo dài (LABA) với thời gian khởi phát tác dụng ngắn và kéo dài tác dụng này ít nhất 24 giờ.
Các thụ thể beta-adrenergic được chia thành 3 phân nhóm, thụ thể beta1-adrenergic phân bố chủ yếu trên cơ tim, thụ thể beta2-adrenergic phân bố chủ yếu trên cơ trơn đường dẫn khí và thụ thể beta3-adrenergic phân bố chủ yếu trên mô mỡ. Các chất chủ vận trên beta2-adrenergic gây giãn phế quản. Mặc dù thụ thể beta2-adrenergic là thụ thể adrenergic chủ yếu trên cơ trơn đường dẫn khí nhưng loại thụ thể này cũng có mặt trên bề mặt nhiều loại tế bào khác, gồm các tế bào biểu mô và nội mô ở phổi và tim. Chức năng rõ ràng của thụ thể beta2-adrenergic trên tim chưa được xác định, tuy nhiên sự có mặt của loại thụ thể này làm tăng khả năng tác dụng trên tim ngay cả chất chủ vận có tính chọn lọc cao trên thụ thể beta2-adrenergic.
Ảnh hưởng trên điện tâm đồ
Tiotropium
Ảnh hưởng của tiotropium (dạng bột hít với liều 18 và 54 microgram một lần mỗi ngày) đến khoảng QT/QTc của điện tâm đồ được thăm dò trong một nghiên cứu ngẫu nhiên, mù đôi, có đối chứng với placebo và với chất hoạt tính (moxifloxacin) trên 56 nam, nữ tình nguyện viên khỏe mạnh. Thay đổi trung bình khoảng QT so với giá trị ban đầu trong khoảng thời gian từ 5 phút đến 2 giờ sau khi sử dụng thuốc vào ngày thứ 12 trung bình là -1,4 mili giây (ms) đối với nhóm placebo, +0,6 mili giây đối với nhóm tiotropium liều 18 microgram và -2,1 mili giây đối với nhóm tiotropium liều 54 microgram; giới hạn trên khoảng tin cậy 95% của khác biệt hiệu chỉnh với placebo so với giá trị ban đầu là dưới 10 mili giây đối với hai mức liều tiotropium(+4,9 mili giây với liều 18 microgram tiotropium, +2,2 mili giây với liều 54 microgram tiotropium).
Olodaterol
Ảnh hưởng của olodaterol đến khoảng QT/QTc trên điện tâm đồ được thăm dò trong một nghiên cứu ngẫu nhiên, mù đôi, có đối chứng với placebo và chứng chất hoạt tính (moxifloxacin) trên 24 nam, nữ tình nguyện viên khỏe mạnh. So với placebo, thay đổi khoảng QT so với giá trị ban đầu tăng phụ thuộc liều, từ 1,6 (10 microgram olodaterol) đến 6,5 mili giây (50 microgram olodaterol), khi sử dụng liều đơn olodaterol 10, 20, 30 và 50 microgram trong khoảng thời gian từ 20 phút đến 2 giờ, với giới hạn trên của khoảng tin cậy 90% hai phía là dưới 10 mili giây ở tất cả các mức liều. Tác dụng của olodaterol 5 microgram và 10 microgram đến nhịp tim và xung nhịp tim được đánh giá bằng đo điện tâm đồ liên tục trong 24 giờ (sử dụng thiết bị giám sát Holter) trên một phân nhóm 772 bệnh nhân trong một thử nghiệm lâm sàng pha 3, có đối chứng với placebo, kéo dài 48 tuần. Không ghi nhận xu hướng phụ thuộc liều hoặc thời gian dùng thuốc đối với mức độ thay đổi trung bình của nhịp tim và ngoại tâm thu. Không có sự khác biệt có ý nghĩa giữa olodaterol liều 5, 10 microgram và placebo về sự thay đổi nhịp ngoại tâm thu từ thời điểm ban đầu đến khi kết thúc quá trình điều trị.
Spiolto Respimat
Trong 2 thử nghiệm lâm sàng ngẫu nhiên, mù đôi, kéo dài 52 tuần, sử dụng SPIOLTO RESPIMAT trên 5162 bệnh nhân COPD, đánh giá điện tâm đồ được thực hiện sau khi dùng thuốc ở ngày thứ 1, 85, 169 và 365. Trong một phân tích gộp, số lượng bệnh nhân có thay đổi trên 30 mili giây khoảng QT so với ban đầu, sử dụng công thức Bazett (QTcB) và Fredericia (QTcF) - công thức hiệu chỉnh QT theo nhịp tim) dao động từ 4,9-6,4% (QTcB) và 3,3-4,7% (QTcF) với nhóm SPIOLTO RESPIMAT so với 5.0-6.0% (QTcB) và 3,4-4,4% (QTcF) với nhóm olodaterol 5 microgram; 5,3-6,5% (QTcB) và 3,0-4,7% (QTcF) với nhóm tiotropium 5 microgram trong tất cả các đánh giá điện tâm đồ đã được thực hiện.
Độ an toàn và hiệu lực lâm sàng
Chương trình phát triển lâm sàng pha III của SPIOLTO RESPIMAT bao gồm 3 thử nghiệm ngẫu nhiên, mù đôi:
(i) Hai thử nghiệm lâm sàng giống nhau, kéo dài 52 tuần, nhóm song song, so sánh SPIOLTO RESPIMAT với tiotropium 5 microgram và olodaterol 5 microgram (1029 bệnh nhân sử dụng SPIOLTO RESPIMAT) [thử nghiệm 1 và 2].
(ii) Một thử nghiệm bắt chéo kéo dài 6 tuần so sánh SPIOLTO RESPIMAT với tiotropium 5 microgram và olodaterol 5 microgram [thử nghiệm 3].
Trong các thử nghiệm này, các thuốc đối chứng tiotropium 5 microgram, olodaterol 5 microgram và placebo được bào chế dưới dạng bình xịt hạt mịn RESPIMAT.
Tất cả các nghiên cứu đều tiến hành đo chức năng phổi (thể tích thở ra gắng sức trong 1 giây, FEV1). Trong các nghiên cứu kéo dài 52 tuần, chức năng phổi được đo trong khoảng thời gian đến 3 giờ sau khi dùng thuốc (12 giờ đối với một phân nhóm bệnh nhân) và tại thời điểm 23-24 giờ sau khi dùng thuốc; những tiêu chí chính về hiệu lực liên quan đến chức năng phổi là thay đổi giá trị AUC0-3giờ của FEV1 và giá trị đáy FEV1 so với trị số tương ứng trước điều trị (đáp ứng) sau 24 tuần. Trong nghiên cứu kéo dài 6 tuần, chức năng phổi được đo trong khoảng thời gian đến 12 giờ sau khi dùng thuốc và tại thời điểm 22-24 giờ sau khi dùng thuốc; tiêu chí chính về hiệu lực là thay đổi AUC0-24giờ của FEV1 sau 6 tuần. Các thử nghiệm kéo dài 52 tuần cũng sử dụng Bộ câu hỏi hô hấp của St. George (SGRQ) làm tiêu chí chính để đánh giá chất lượng cuộc sống liên quan đến sức khỏe và sử dụng Chỉ số khó thở chuyển tiếp Mahler (TDI) làm tiêu chí phụ then chốt để đánh giá triệu chứng khó thở.
Các bệnh nhân tham gia vào chương trình nghiên cứu pha III có độ tuổi ≥ 40 với chẩn đoán lâm sàng mắc COPD, có tiền sử hút thuốc trên 10 gói năm, đồng thời có mức độ suy giảm chức năng phổi trung bình đến rất nặng (FEV1 sau khi sử dụng thuốc giãn phế quản nhỏ hơn 80% so với dự đoán (giai đoạn 2-4 theo phân loại GOLD); tỷ lệ FEV1/FVC sau khi sử dụng thuốc giãn phế quản nhỏ hơn 70%).
Các đặc điểm về bệnh nhân
Phần lớn trong số 5162 bệnh nhân trên toàn thế giới tham gia vào hai thử nghiệm kéo dài 52 tuần [thử nghiệm 1 và 2] là nam giới (73%), người da trắng (71%) hoặc người châu Á (25%), có độ tuổi trung bình là 64. Giá trị FEV1 trung bình sau khi sử dụng thuốc giãn phế quản là 1,37 L (GOLD 2 [50%], GOLD 3 [39%] và GOLD 4 [11%]. Đáp ứng với thuốc chủ vận beta2 trung bình là 16,6% so với trị số ban đầu (0,171 L). Các thuốc hô hấp được sử dụng trong phác đồ kết hợp bao gồm steroid dạng hít [47%] và xanthine [10%].
Thử nghiệm kéo dài 6 tuần [thử nghiệm 3] được thực hiện ở Châu Âu và Bắc Mỹ. Phần lớn trong số 219 bệnh nhân tham gia là nam giới (59%), da trắng (99%) và có độ tuổi trung bình là 61,1. Giá trị FEV1 trung bình sau khi sử dụng thuốc giãn phế quản là 1,55 L (GOLD 2 [64%], GOLD 3 [34%] và GOLD 4 [2%]. Đáp ứng với thuốc chủ vận beta2 trung bình là 15,9 % so với trị số ban đầu (0,193 L). Các thuốc hô hấp được sử dụng trong phác đồ kết hợp bao gồm các steroid dạng hít [41%] và xanthine [4%].
Chức năng phổi
Trong các thử nghiệm kéo dài 52 tuần, SPIOLTO RESPIMAT dùng 1 lần mỗi ngày vào buổi sáng đã cho thấy khả năng cải thiện chức năng phổi rõ rệt trong 5 phút sau khi sử dụng liều đầu tiên so với tiotropium 5 microgram (SPIOLTO RESPIMAT làm tăng FEV1 trung bình 0,137 L so với 0,058 L của tiotropium 5 microgram [p < 0,0001] và 0,125 L olodaterol 5 microgram [p=0,16]). Trong cả 2 nghiên cứu, những cải thiện đáng kể đã được ghi nhận với SPIOLTO RESPIMAT so với tiotropium 5 microgram và olodaterol 5 microgram, thể hiện ở mức độ thay đổi AUC0-3giờ của FEV1 và giá trị đáy FEV1 sau 24 tuần (tiêu chí chính đánh giá chức năng phổi).

Tác dụng giãn phế quản của SPIOLTO RESPIMAT mạnh hơn so với tiotropium 5 microgram và olodaterol 5 microgram trong suốt 52 tuần điều trị. SPIOLTO RESPIMAT cũng cải thiện PEFR (tốc độ độ thở ra tối đa) vào buổi sáng và buổi tối so với tiotropium 5 microgram và olodaterol 5 microgram, theo số liệu được ghi nhận hàng ngày từ bệnh nhân.
Trong phân nhóm bệnh nhân được đo chức năng phổi sau khi dùng thuốc trong thời gian lên tới 12 giờ, SPIOLTO RESPIMAT thể hiện mức độ thay đổi FEV1 lớn hơn đáng kể so với tiotropium 5 microgram và olodaterol 5 microgram trong suốt khoảng thời gian 24 giờ giữa hai lần dùng thuốc.
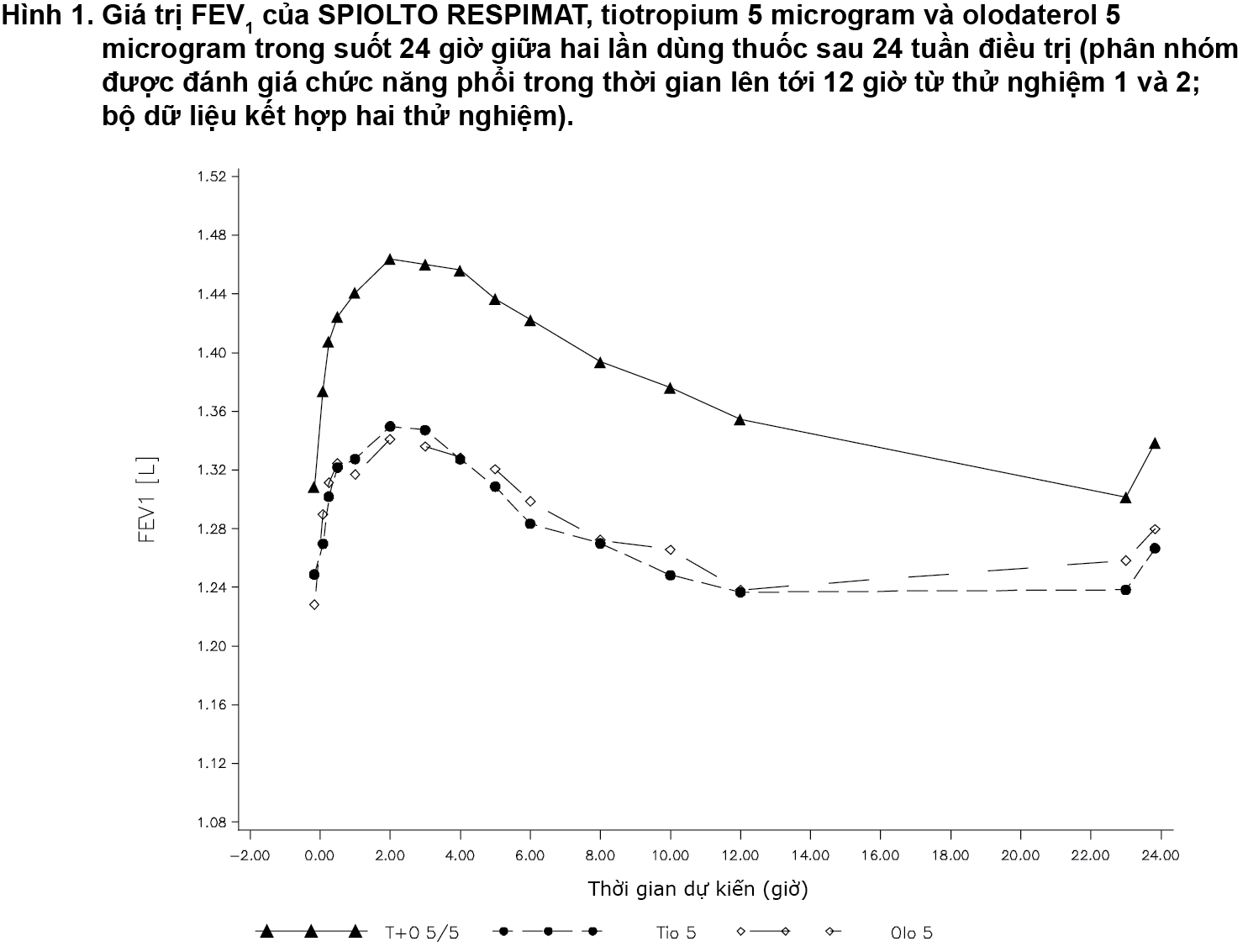

Trong thử nghiệm lâm sàng kéo dài 6 tuần, SPIOLTO RESPIMAT có giá trị FEV1 cao hơn đáng kể so với tiotropium 5 microgram, olodaterol 5 microgram và placebo trong suốt 24 giờ giữa hai lần dùng thuốc.
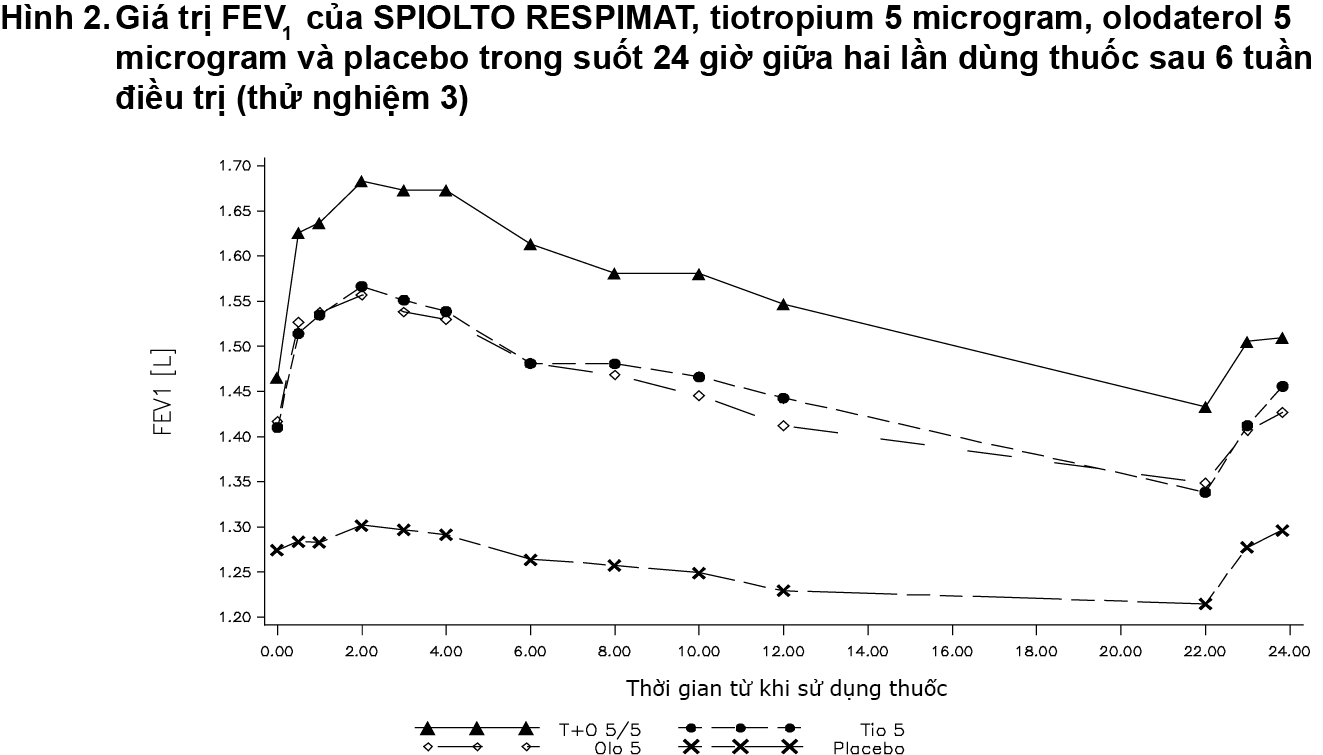
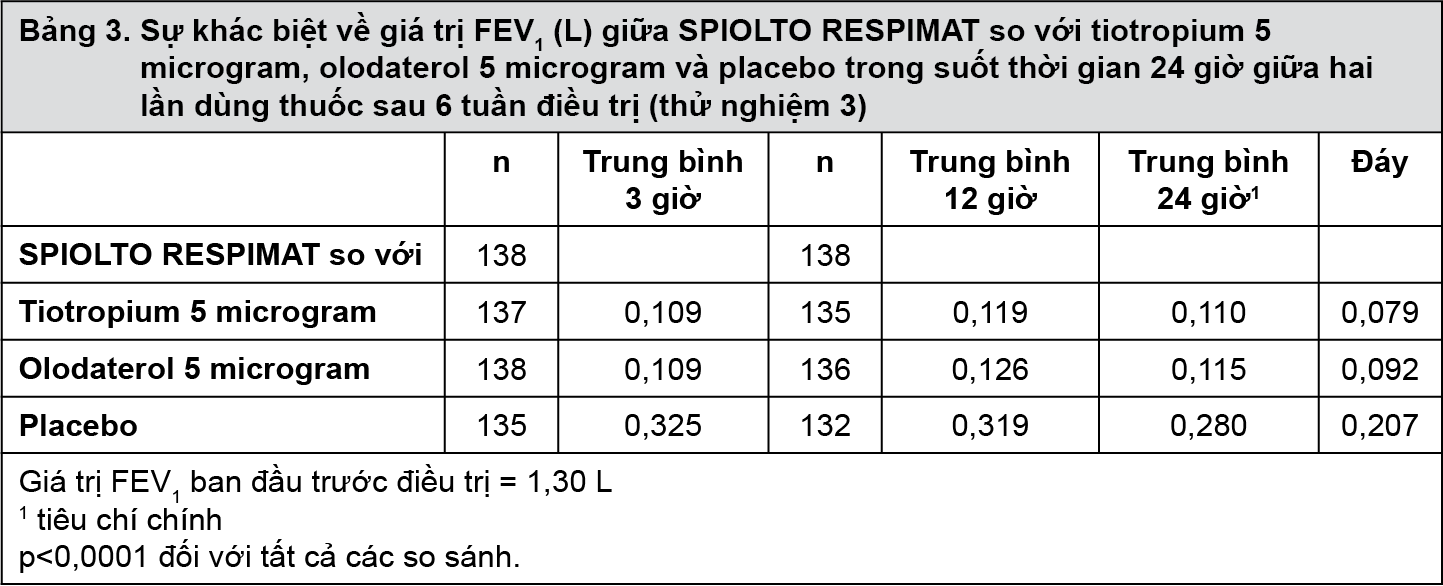
Chất lượng cuộc sống liên quan đến sức khỏe
Sau 24 tuần, SPIOLTO RESPIMAT cải thiện đáng kể tổng điểm SGRQ trung bình so với tiotropium 5 microgram và olodaterol 5 microgram (bảng 4); sự cải thiện được ghi nhận ở tất cả các nhóm tiêu chí của thang SGRQ. Số lượng bệnh nhân sử dụng SPIOLTO RESPIMAT có sự cải thiện tổng điểm SGRQ có ý nghĩa lâm sàng (MCID, được định nghĩa là sự giảm ít nhất 4 điểm so với ban đầu) lớn hơn so với nhóm sử dụng tiotropium 5 microgram (57,5% so với 48,7% , p=0,0001) và olodaterol 5 microgram (57,5% so với 44,8%, p < 0,0001).
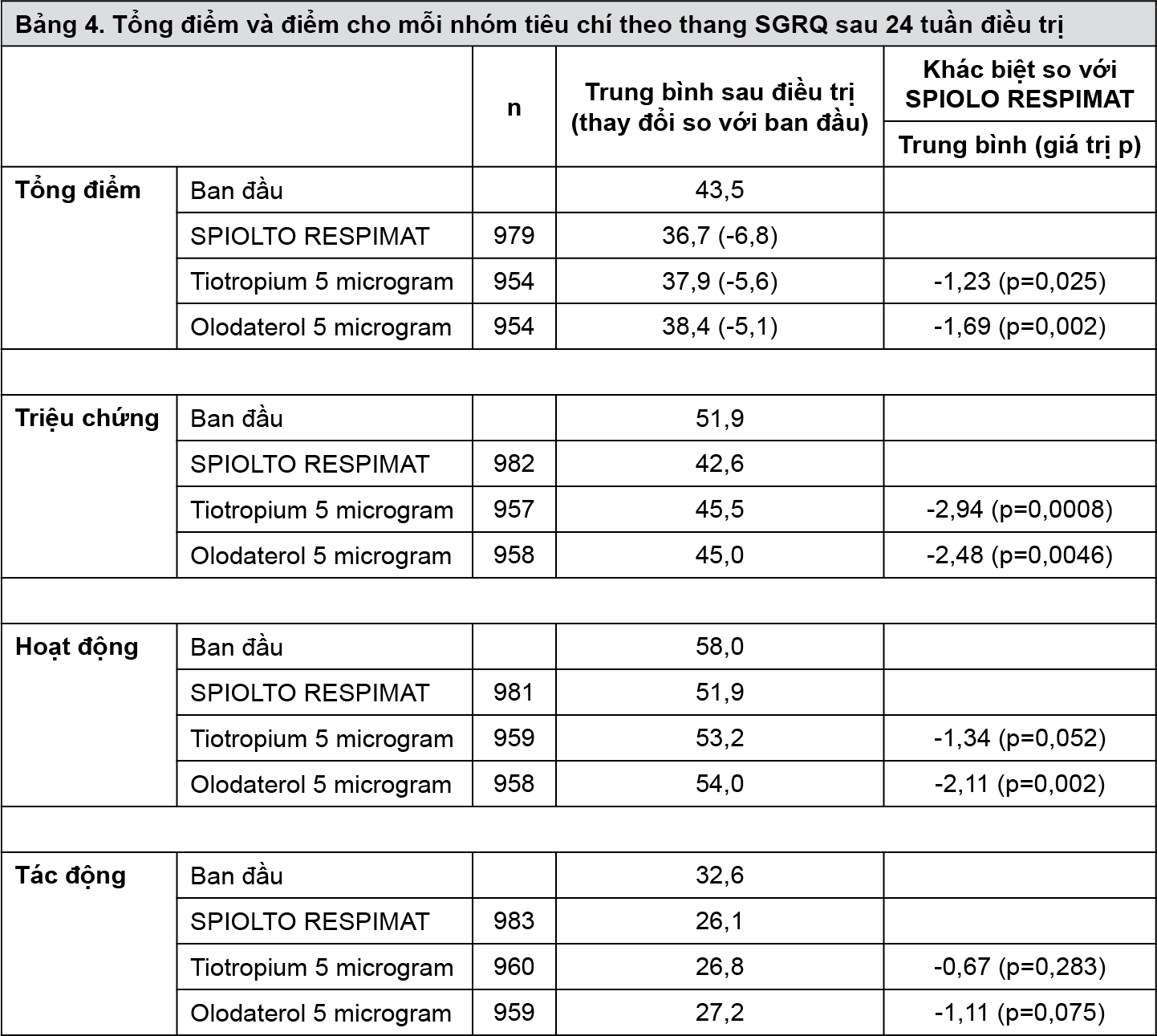
Khó thở
Sau 24 tuần, SPIOLTO RESPIMAT cải thiện đáng kể điểm trung bình TDI chính (TDI focal score) so với tiotropium 5 microgram và olodaterol 5 microgram (bảng 5). Số lượng bệnh nhân sử dụng SPIOLTO RESPIMAT cải thiện có ý nghĩa lâm sàng điểm TDI chính (MCID, được định nghĩa là giá trị ≥ 1) hơn so với tiotropium 5 microgram (54,9% so với 50,6%, p=0,0546) và olodaterol 5 microgram (54,9% so với 48,2%, p=0,0026).

Sử dụng thuốc cắt cơn
Nhu cầu sử dụng thuốc cắt cơn salbutamol vào ban ngày và ban đêm đối với bệnh nhân được điều trị bằng SPIOLTO RESPIMAT ít hơn so với bệnh nhân được điều trị bằng tiotropium 5 microgram and olodaterol 5 microgram.
Xếp hạng toàn cầu từ bệnh nhân (PGR)
Các bệnh nhân sử dụng SPIOLTO RESPIMAT có sự cải thiện tình trạng hô hấp rõ rệt hơn so với tiotropium 5 microgram và olodaterol 5 microgram theo thang Đánh Giá Toàn Cầu Từ Bệnh Nhân (PGR).
Đợt kịch phát
Trước đây, tiotropium 5 microgram đã được chứng minh làm giảm có ý nghĩa thống kê nguy cơ xuất hiện đợt kịch phát COPD so với placebo. Đợt kịch phát COPD được coi là tiêu chí bổ sung trong hai thử nghiệm then chốt kéo dài 52 tuần (thử nghiệm 1 và 2). Trong bộ dữ liệu kết hợp hai thử nghiệm, tỷ lệ bệnh nhân trải qua đợt kịch phát COPD trung bình/nặng là 27,7% với nhóm SPIOLTO RESPIMAT và 28,8% với nhóm tiotropium 5 microgram.
Dung tích hít vào, cảm giác khó thở và khả năng dung nạp gắng sức
Ảnh hưởng của SPIOLTO RESPIMAT đến dung tích hít vào, cảm giác khó thở và dung nạp gắng sức giới hạn bởi triệu chứng được nghiên cứu trong 3 thử nghiệm lâm sàng ngẫu nhiên, mù đôi trên bệnh nhân COPD:
(i) Hai thử nghiệm bắt chéo, lặp lại, kéo dài 6 tuần, so sánh SPIOLTO RESPIMAT với tiotropium 5 microgram, olodaterol 5 microgram và placebo trong nghiệm pháp đạp xe tốc độ hằng định (450 bệnh nhân sử dụng SPIOLTO RESPIMAT) [thử nghiệm 4 và 5].
(ii) Một thử nghiệm nhóm song song kéo dài 12 tuần so sánh SPIOLTO RESPIMAT với placebo trong nghiệm pháp đạp xe tốc độ hằng định (139 bệnh nhân sử dụng SPIOLTO RESPIMAT) và nghiệm pháp đi bộ tốc độ hằng định (một phân nhóm bệnh nhân) [thử nghiệm 6].
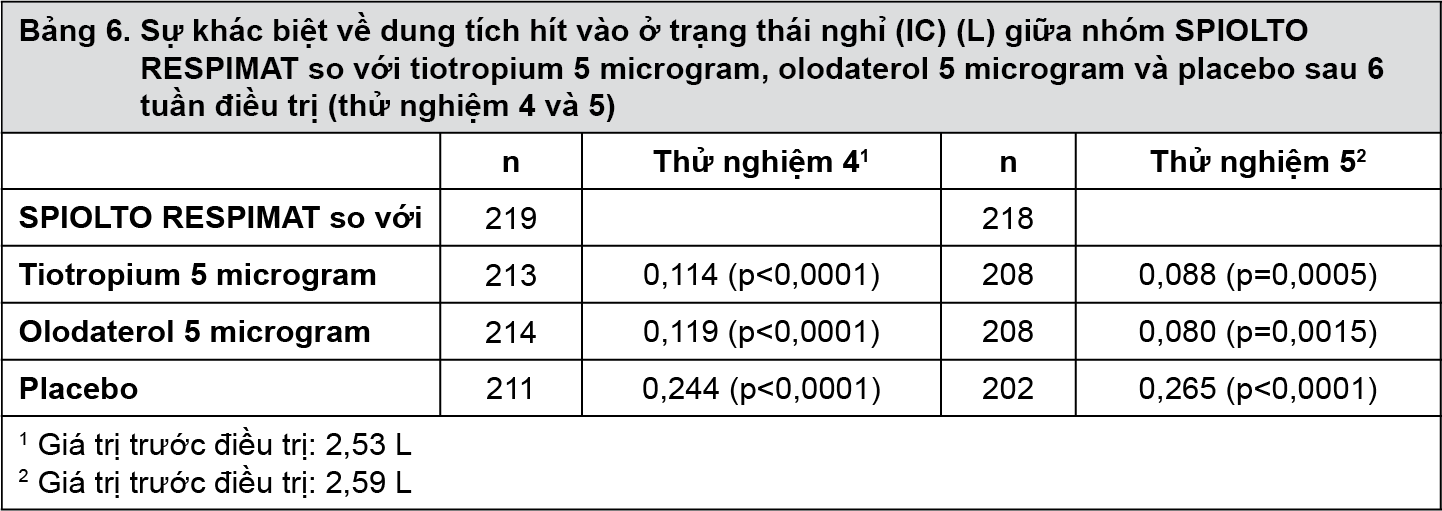
SPIOLTO RESPIMAT cải thiện đáng kể dung tích hít vào so với tiotropium 5 microgram, olodaterol 5 microgram và placebo sau 6 tuần điều trị (thử nghiệm 4 và 5; bảng 6) và so với placebo sau 12 tuần điều trị (0,234 L, p < 0,0001; thử nghiệm 6).
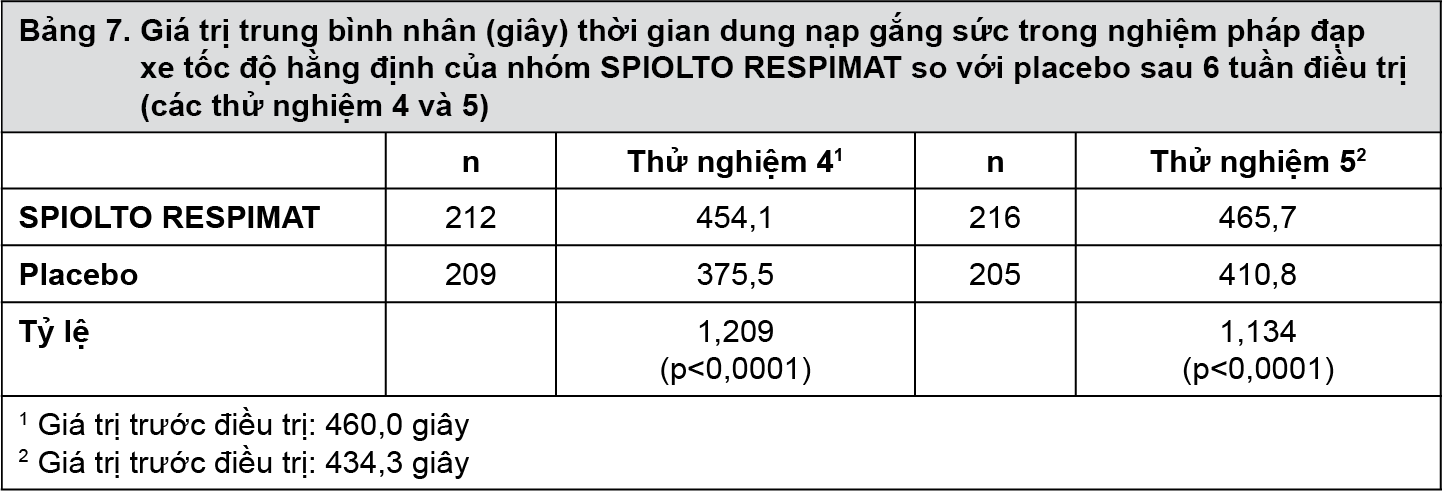
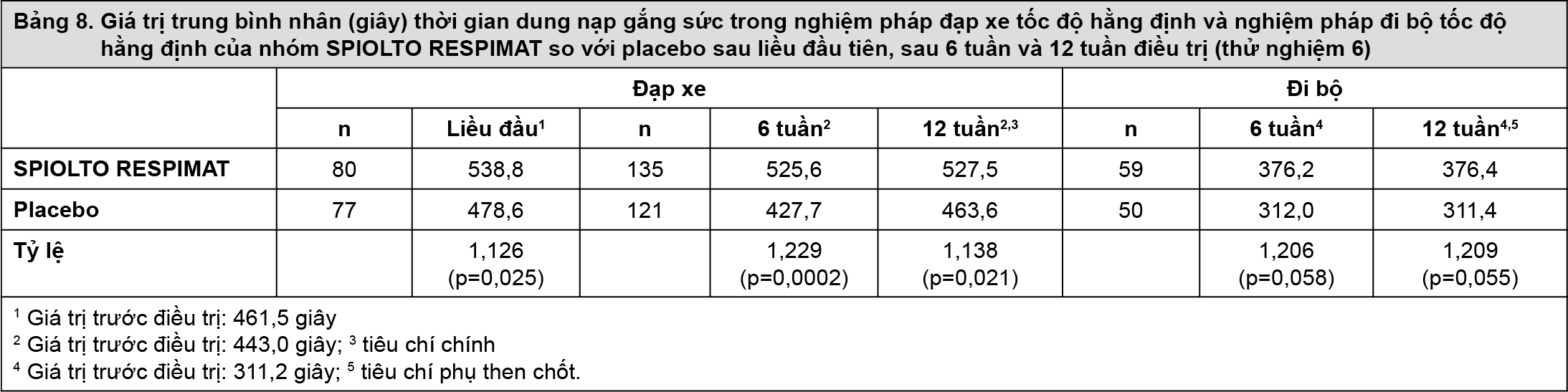
Trong các thử nghiệm 4 và 5, SPIOLTO RESPIMAT đã cải thiện thời gian dung nạp gắng sức trong nghiệm pháp đạp xe tốc độ hằng định lần lượt là 20,9% và 13,4% so với placebo (bảng 7). Trong thử nghiệm 6, SPIOLTO RESPIMAT đã cải thiện thời gian dung nạp gắng sức trong nghiệm pháp đạp xe tốc độ hằng định khoảng 12,6% sau liều đầu tiên (trong một phân nhóm bệnh nhân), khoảng 22,9% sau 6 tuần điều trị và 13,8% sau 12 tuần điều trị so với placebo; tăng thời gian dung nạp gắng sức trong nghiệm pháp đi bộ tốc độ hằng định (trong một phân nhóm bệnh nhân) khoảng 20,6% sau 6 tuần điều trị và 20,9% sau 12 tuần điều trị so với placebo (bảng 8).
Trong các thử nghiệm 4 và 5, SPIOLTO RESPIMAT làm giảm độ dốc của cảm giác khó thở trong nghiệm pháp đạp xe tốc độ hằng định so với placebo sau 6 tuần điều trị (p < 0.0005; bảng 9).

Đặc điểm dược động học
Khi sử dụng tiotropium kết hợp với olodaterol theo đường hít, các thông số dược động học của mỗi thành phần tương tự như khi chúng được sử dụng riêng rẽ.
Dược động học của tiotropium và olodaterol tuyến tính trong khoảng liều điều trị. Sử dụng liều lặp lại 1 lần mỗi ngày theo đường hít, trạng thái ổn định của tiotropium đạt được sau 7 ngày. Trạng thái ổn định của olodaterol đạt được sau 8 ngày sử dụng liều 1 lần mỗi ngày theo đường hít và tích lũy thuốc lên đến 1,8 lần so với liều đơn.
Hấp thu
Tiotropium: Dữ liệu về bài tiết thuốc qua nước tiểu trên người tình nguyện khỏe mạnh trẻ tuổi cho thấy khoảng 33% liều hít vào từ bình xịt hạt mịn RESPIMAT được hấp thu vào tuần hoàn. Sinh khả dụng tuyệt đối của dung dịch uống khoảng 2-3%. Nồng độ tối đa của tiotropium trong huyết tương đạt được sau 5-7 phút sử dụng bình xịt hạt mịn RESPIMAT.
Olodaterol: Trên người tình nguyện khỏe mạnh, sinh khả dụng tuyệt đối của olodaterol sau khi dùng dạng hít ước tính khoảng 30%, trái lại, sinh khả dụng tuyệt đối khi dùng dạng dung dịch uống là dưới 1%. Nồng độ tối đa của olodaterol trong huyết tương đạt được sau 10 đến 20 phút sử dụng bình xịt hạt mịn RESPIMAT.
Phân bố
Tiotropium kết hợp với protein huyết tương khoảng 72% và có thể tích phân bố là 32 L/kg. Các nghiên cứu trên chuột cống cho thấy tiotropium không thấm qua hàng rào máu não ở bất kỳ mức độ nào.
Olodaterol liên kết với protein huyết tương khoảng 60% và có thể tích phân bố 1110 L.
Chuyển hóa sinh học
Tiotropium: Ít được chuyển hóa. Điều này được thấy rõ khi có tới 74% liều dùng đường tĩnh mạch được thải trừ trong nước tiểu dưới dạng không biến đổi. Phản ứng phân cắt liên kết ester của tiotropium không cần enzym xúc tác, tạo ra hợp chất chứa nhóm alcol và phần acid tương ứng (N-methylscopine và acid dithienylglycolic), cả 2 thành phần này đều không gắn kết với thụ thể muscarinic. Thực nghiệm in vitro với microsome và tế bào gan người cho thấy một lượng thuốc (< 20% liều dùng đường tĩnh mạch) được chuyển hóa bằng quá trình oxy hóa phụ thuộc cytochrome P450 (CYP) 2D6 và 3A4, sau đó liên hợp với glutathione để tạo thành nhiều chất chuyển hóa pha II khác nhau.
Olodaterol: Được chuyển hóa chính bằng con đường glucuronic hoá trực tiếp và O-demethyl hóa ở nhóm methoxy kèm theo phản ứng liên hợp sau đó. Trong 6 chất chuyển hóa đã được xác định, chỉ có sản phẩm demethyl hóa ở dạng chưa liên hợp (SOM 1522) có khả năng liên kết với thụ thể beta2; tuy nhiên, không phát hiện được chất chuyển hóa này trong huyết tương sau khi dùng lặp lại nhiều lần liều khuyến cáo hoặc lên tới 4 lần liều khuyến cáo. Các isozyme của cytochrome P450 bao gồm CYP2C9, CYP3C8 cùng với đóng góp không đáng kể của CYP3A4, xúc tác cho phản ứng demethyl hóa olodaterol, trong khi các isoform của uridine diphosphate glycosyl transferase gồm UGT2B7, UGT1A1, 1A7 và 1A9 xúc tác tạo thành olodaterol - glucuronide.
Thải trừ
Tiotropium: Tiotropium đường tĩnh mạch được thải trừ chủ yếu bằng bài tiết nguyên vẹn qua nước tiểu (74%). Độ thanh thải toàn phần trên người tình nguyện khỏe mạnh là 880mL/phút. Khi dùng dạng hít trên bệnh nhân COPD, tại trạng thái ổn định có 18,6% liều dùng được bài tiết qua nước tiểu, phần còn lại chủ yếu là lượng thuốc không được hấp thu tại ruột và được thải trừ qua phân. Độ thanh thải của tiotropium qua thận lớn hơn tốc độ lọc của cầu thận, chứng tỏ có quá trình bài tiết chủ động thuốc vào trong nước tiểu. Nửa đời thải trừ của tiotropium sau khi dùng dạng xịt trên bệnh nhân COPD khoảng 27 đến 45 giờ.
Olodaterol: Độ thanh thải toàn phần của olodaterol trên người tình nguyện khỏe mạnh là 872mL/phút, và độ thanh thải của thận là 173mL/phút. Nửa đời thải trừ sau khi dùng đường tĩnh mạch là 22 giờ. Trái lại, nửa đời thải trừ sau khi dùng dạng hít là khoảng 45 giờ, chứng tỏ giá trị này chịu ảnh hưởng của quá trình hấp thu lớn hơn so với quá trình thải trừ.
Sau khi dùng olodaterol gắn đồng vị 14C theo đường tĩnh mạch, 38% liều gắn chất phóng xạ được tìm thấy trong nước tiểu và 53% được tìm thấy trong phân. Lượng olodaterol nguyên vẹn được tìm thấy trong nước tiểu sau khi dùng đường tĩnh mạch là 19%. Sau khi uống, chỉ 9% chất gắn phóng xạ được tìm thấy trong nước tiểu, trong khi một lượng lớn được tìm thấy trong phân (84%). Sau khi dùng đường tĩnh mạch và đường uống, trên 90% liều được bài tiết trong tương ứng 6 ngày và 5 ngày. Sau khi dùng dạng hít, tại trạng thái ổn định, lượng olodaterol nguyên vẹn được bài tiết qua nước tiểu trong khoảng thời gian giữa hai lần dùng thuốc trên người tình nguyện khỏe mạnh ước tính khoảng 5-7% liều dùng.
Đặc điểm bệnh nhân
Tiotropium
Tương tự tất cả các thuốc được thải trừ chủ yếu qua thận, tuổi cao liên quan đến giảm độ thanh thải thận của tiotropium trên bệnh nhân COPD từ 347mL/phút với người dưới 65 tuổi xuống còn 275mL/phút với người ≥ 65 tuổi. Điều này không làm tăng tương ứng giá trị AUC0-6,ss hoặc giá trị Cmax,ss.
Olodaterol
Một phân tích tổng hợp dược động học sử dụng dữ liệu từ 2 thử nghiệm lâm sàng có đối chứng trên 405 bệnh nhân COPD và 296 bệnh nhân hen cho thấy không cần hiệu chỉnh liều khi xem xét ảnh hưởng của tuổi tác, giới tính, và cân nặng đến sự phơi nhiễm olodaterol toàn thân.
So sánh dữ liệu dược động học giữa các nghiên cứu về olodaterol chỉ ra xu hướng phơi nhiễm toàn thân ở người Nhật Bản và người Châu Á cao hơn so với người da trắng.
Không có những vấn đề liên quan đến độ an toàn được ghi nhận trong các nghiên cứu lâm sàng khi sử dụng olodaterol trên người da trắng và người Châu Á với mức liều cao hơn 2 lần mức liều khuyến cáo trong thời gian lên đến một năm.
Suy thận
Tiotropium: Sau khi sử dụng tiotropium dạng hít một lần mỗi ngày trên bệnh nhân COPD kèm suy thận nhẹ (CLCR 50-80mL/phút), tại trạng thái ổn định, giá trị AUC0-6,ss tăng nhẹ (cao hơn 1,8 đến 30%) và Cmax,ss không thay đổi so với bệnh nhân có chức năng thận bình thường (CLCR >80mL/phút). Trên bệnh nhân suy thận trung bình và nặng (CLCR < 50mL/phút) sử dụng tiotropium đường tĩnh mạch, phơi nhiễm toàn thân cao gấp 2 lần (AUC0-4giờ tăng 82% và Cmax tăng 52%) so với bệnh nhân có chức năng thận bình thường, điều này đã được xác nhận với dạng bột khô để hít.
Olodaterol: Trên bệnh nhân suy thận nặng (CLCR < 30mL/phút), phơi nhiễm toàn thân khi sử dụng olodaterol tăng trung bình 1,4 lần. Mức độ tăng phơi nhiễm này không làm tăng bất kỳ vấn đề nào liên quan đến độ an toàn, được chứng minh thông qua dữ liệu về độ an toàn khi sử dụng olodaterol trong những nghiên cứu lâm sàng kéo dài lên tới một năm với liều lên tới hai lần liều khuyến cáo.
Suy gan
Tiotropium: Suy giảm chức năng gan được dự đoán không có bất kỳ ảnh hưởng nào đến được động học của tiotropium.
Tiotropium được thải trừ chủ yếu qua thận (74% trên người tình nguyện khỏe mạnh) và được phân cắt ester đơn giản không cần enzym xúc tác để tạo thành các sản phẩm không có tác dụng dược lý.
Olodaterol: Trên bệnh nhân suy gan nhẹ và trung bình, phơi nhiễm toàn thân khi sử dụng olodaterol không bị ảnh hưởng. Ảnh hưởng của suy gan nặng đến mức độ phơi nhiễm toàn thân khi sử dụng olodaterol chưa được nghiên cứu.
Các tương tác thuốc - thuốc
Olodaterol: Các nghiên cứu tương tác thuốc - thuốc đã được thực hiện, sử dụng fluconazole làm chất ức chế CYP 2C9 và ketoconazole làm chất ức chế đồng thời CYP và P-gp.
Fluconazole: Sử dụng đồng thời fluconazole 400 mg một lần/ngày trong 14 ngày không ảnh hưởng đáng kể đến phơi nhiễm toàn thân của olodaterol.
Ketoconazole: Sử dụng đồng thời ketoconazole 400 mg một lần/ngày trong 14 ngày làm tăng Cmax và AUC0-1 của olodaterol lần lượt là 66% và 68%.