Thành phần
Mỗi viên nén bao phim chứa:
Hoạt chất: Itoprid HCI 50mg
Tá dược: Lactose monohydrat, tinh bột ngô, natri crosscarmellose, silic oxyd dạng keo khan, magnesi stearat, opadry II white.
Công dụng (Chỉ định)
Chữa trị những triệu chứng về dạ dày-ruột gây ra bởi viêm dạ dày mạn (cảm giác đầy chướng bụng, đau bụng trên, chán ăn, ợ nóng, buồn nôn và nôn).
Cách dùng - Liều dùng
Liều uống thông thường cho người lớn là 150 mg itoprid hydrochlorid (3 viên) mỗi ngày, chia 3 lần, mỗi lần 1 viên, uống trước bữa ăn. Liều này có thể giảm bớt tùy thuộc vào tuổi tác và bệnh trạng của từng bệnh nhân.
Không sử dụng trong trường hợp sau (Chống chỉ định)
Chống chỉ định cho những bệnh nhân có tiền sử mẫn cảm với bất kỳ thành phần nào của thuốc. Không dùng cho phụ nữ có thai hoặc cho con bú trừ khi thực sự cần thiết.
Lưu ý khi sử dụng (Cảnh báo và thận trọng)
Cảnh báo quan trọng
- Nên lưu ý khi sử dụng vì thuốc này làm tăng hoạt tính của acetylcholin.
- Không nên dùng kéo dài khi không thấy có sự cải thiện về những triệu chứng của dạ dày-ruột.
Sử dụng thuốc cho người cao tuổi: Vì chức năng sinh lý ở người cao tuổi giảm nên những tác dụng không mong muốn dễ xảy ra hơn. Do đó, những bệnh nhân cao tuổi sử dụng thuốc này nên được theo dõi cẩn thận, nếu có bất kỳ tác dụng không mong muốn nào xuất hiện, nên sử dụng những biện pháp xử trí thích hợp, ví dụ như giảm liều hoặc ngừng thuốc.
Sử dụng trong nhi khoa: Độ an toàn của thuốc trên trẻ em vẫn chưa được xác định (Còn có ít bằng chứng lâm sàng).
Không dùng thuốc khi quá hạn sử dụng.
Tác dụng không mong muốn (Tác dụng phụ)
Tại thời điểm thuốc gốc được cấp phép lưu hành tại Nhật: Những tác dụng không mong muốn được thấy ở 14 (2,45%) trên 572 bệnh nhân (19 trường hợp, 3,32%). Tác dụng không mong muốn chủ yếu là tiêu chảy (4 trường hợp; 0,7%), đau đầu (2 trường hợp; 0,35%), đau bụng (2 trường hợp, 0,35%). Những bất thường về các dữ liệu xét nghiệm là giảm bạch cầu (4 trường hợp), tăng prolactin (2 trường hợp),...
Tại thời điểm đánh giá lại: Những tác dụng không mong muốn được thấy ở 74 (1,25%) trên 5913 bệnh nhân (104 trường hợp; 1,76%). Những tác dụng không mong muốn chính có bất thường về các dữ liệu xét nghiệm là tiêu chảy (13 trường hợp; 0,22%), đau bụng (8 trường hợp; 0,14%), táo bón (8 trường hợp; 0,14%), tăng AST (GOT) (8 trường hợp; 0,14%), tăng ALT (GPT) (8 trường hợp; 0,14%).....
Những tác dụng không mong muốn có ý nghĩa lâm sàng
- Sốc và phản ứng quá mẫn (tỉ lệ mắc chưa được biết): Sốc và phản ứng quá mẫn có thể xuất hiện, và nên theo dõi bệnh nhân chặt chẽ. Nêu thấy bất kỳ dấu hiệu nào của sốc và phản ứng quá mẫn, ví dụ như tụt huyết áp, khó thở, phù thanh quản, nổi mề đay, tái nhợt và toát mồ hôi.... nên ngừng ngay thuốc và có những biện pháp điều trị thích hợp.
- Rối loạn chức năng gan và vàng da (tỉ lệ mắc chưa được biết): Rối loạn chức năng gan và vàng da cùng với tăng AST (GOT), ALT (GPT) và y-GTP ... có thể xuất hiện và bệnh nhân nên được theo dõi chặt chẽ. Nếu phát hiện thấy những triệu chứng bất thường trên nên ngừng ngay thuốc và có những biện pháp điều trị thích hợp.
Những tác dụng khống mong muốn khác (AR):
|
|
0,1% ≤ AR ≤ 5%
|
AR <0,1%
|
Tỉ lệ mắc chưa biết (1)
|
|
Quá mẫn (2)
|
|
|
Phát ban, mẫn đỏ, ngứa...
|
|
Triệu chứng ngoại tháp (2)
|
|
Run rẩy...
|
|
|
Nội tiết (2)
|
|
Tăng prolactin,...
|
Chứng to vú ở đàn ông
|
|
Huyết học (2)
|
|
Giảm tiểu cầu, giảm bạch cầu...
|
|
|
Đuờng tiêu hóa
|
Tiêu chảy, táo bón, đau bụng...
|
Buồn nôn, tăng tiết nước bọt...
|
|
|
Tâm thần
|
|
Đau đầu, cảm giác khó chịu, rối loạn giấc ngủ, chóng mặt...
|
|
|
Gan
|
Tăng AST (GOT), tăng ALT (GPT)...
|
Tăng γ-GTP, tăng Al-P,...
|
|
|
Thận
|
|
Tăng BUN, tăng creatinin...
|
|
|
Các loại khác
|
|
Đau lưng hoặc ngực, mệt mỏi...
|
|
Ghi chú:
(1) Tỉ lệ mắc chưa được biết do đây là những báo cáo tự phát
(2) Nếu có bất kỳ dấu hiệu bất thường nào được phát hiện, nên có những biện pháp xử trí thích hợp, ví dụ như ngưng dùng thuốc...
Thông báo cho bác sĩ những tác dụng không mong muôn gặp phải khi sử dụng thuốc.
Tương tác với các thuốc khác
Nên lưu ý khi dùng kết hợp IBUTOP với những thuốc sau: Dùng đổng thời itoprid hydrochlorid với các thuốc kháng cholinergic như: Tiquizium bromide, scopolamine butyl bromide, timepidium bromide,... có thể làm giảm tác dụng tăng nhu động dạ dày-ruột của itoprid (tác dụng cholinergic), do tác dụng ức chế của những thuốc kháng cholinergic có thể có tác dụng dược lý học đối kháng tác dụng của itoprid.
Quá liều
Chưa có báo cáo về trường hợp quá liều ở người. Trong trường hợp quá liều nghiêm trọng, các biện pháp thông thường như rửa dạ dày và điều trị triệu chứng nên được áp dụng.
Lái xe và vận hành máy móc
Tác dụng không mong muốn như chóng mặt có thể xảy ra. Khả năng lái xe và vận hành máy móc có thể bị giảm xuống.
Thai kỳ và cho con bú
- Thuốc này chỉ nên sử dụng ở phụ nữ có thai, hoặc ở phụ nữ có thể mang thai chỉ khi lợi ích mong muốn của trị liệu lớn hơn những rủi ro có thể gặp phải (Sự an toàn của sản phẩm này ở phụ nữ có thai vẫn chưa được xác định).
- Tốt nhất là không nên sử dụng thuốc này trong thời kỳ cho con bú, nhưng nếu cần thiết, tránh cho con bú trong quá trình điều trị. Đã có báo cáo cho thấy itoprid hydrochlorid được bài tiết qua sữa ở những thí nghiệm trên động vật (chuột cống).
Bảo quản
Ở nhiệt độ dưới 30°C, nơi khô ráo, tránh ánh sáng.
Quy cách đóng gói
Hộp 2 vỉ x 10 viên nén bao phim.
Hạn dùng
36 tháng kể từ ngày sản xuất.
Dược lực học
Cơ chế tác dụng: Itoprid hydrochlorid làm tăng sự giải phóng acetylcholin (ACh) do tác dụng đối kháng với thụ thể D2 dopamin, và ức chế sự phân hủy acetylcholin được giải phóng qua việc ức chế acetylcholin esterase, dẫn đến làm tăng nhu động dạ dày-ruột.
Làm tăng nhu động dạ dày-ruột:
- Làm tăng nhu động dạ dày. Itoprid hydrochlorid làm tăng nhu động dạ dày của chó lúc thức, phụ thuộc vào liều.
- Tăng khả năng làm rỗng dạ dày. Itoprid hydrochlorid làm tăng khả năng rỗng dạ dày ở người, chó, chuột cống.
Làm giảm nôn: Itoprid hydrochlorid ức chế nôn ở chó gây ra bởi apomorphin, tác dụng này phụ thuộc vào liều.
Dược động học
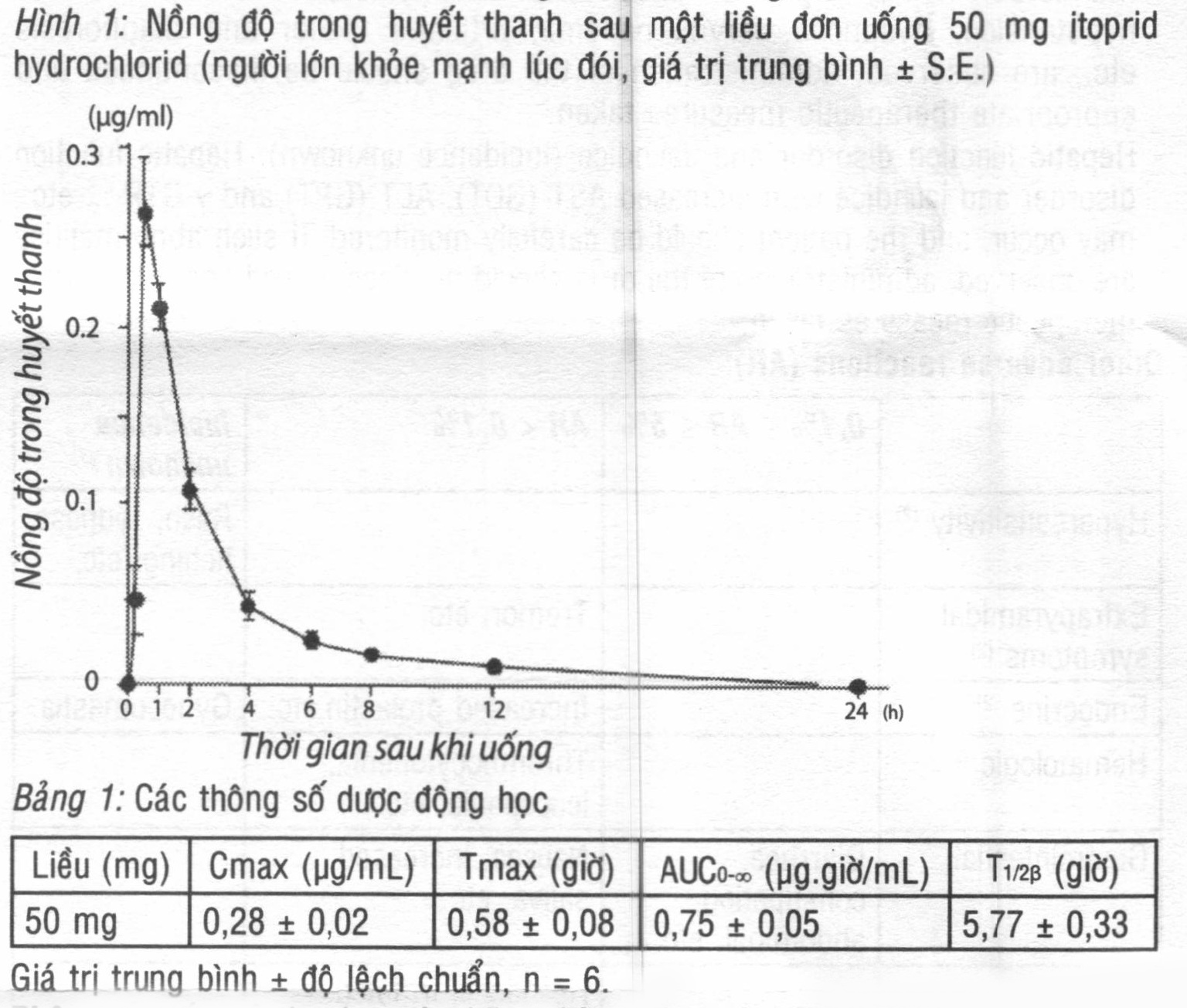
Nồng độ trong huyết thanh: Nồng độ trong huyết thanh và những thông số dược động học ở người lớn khỏe mạnh, sau một liều đơn uống 50 mg itoprid hydrochlorid lúc đói đuợc chỉ rõ trong hình 1 và bảng 1:
Phân bố: Kết quả thu được từ những thí nghiệm trên động vật
- Nồng độ tối đa đạt được ở hầu hết tất cả các mô từ 1 đến 2 giờ sau liều uống đơn 5 mg/kg 14C-itoprid hydrochlorid ở chuột cống, và 2 giờ sau khi uống đạt nồng độ cao ở thận, ruột non, gan, tuyến thượng thận, dạ dày (theo mức độ giảm dần từ cao xuống thấp) và phần thuốc đi vào hệ thống thần kinh trung ương, như não và tủy sống, là rất ít.
- Khi đưa 14C-itoprid hydrochlorid với liều 5 mg/kg vào tá tràng chuột cống, nồng độ hoạt tính phóng xạ trong những lớp cơ dạ dày cao hơn khoảng 2 lần so với nồng độ trong máu.
- Sự bài tiết qua sữa: khi dùng liều uống 5 mg/kg 14C-itoprid hydrochlorid cho chuột cống, nồng độ hoạt tính phóng xạ trong sữa so với trong huyết thanh cao hơn 1,2 lần về Cmax, 2,6 lần cao hơn về AUC, và 2,1 lần cao hơn về T1/2.
Tỉ lệ liên kết protein huyết thanh là 96% sau khi dùng liều đơn uống 100 mg itoprid hydrochlorid cho người khỏe mạnh (6 nam giới) khi đói.
Chuyển hóa và thải trừ:
- Ở liều uống đơn 100 mg itoprid hydrochlorid dùng cho người lớn khỏe mạnh (6 nam giới) khi đói, tỷ lệ bài tiết qua nước tiểu trong vòng 24 giờ sau khi uống cao nhất là dạng N-oxide [67,54% của liều dùng (89,41% của phần bài tiết qua nước tiểu)] và sau đó là dạng thuốc không đổi (4,14%), và những chất còn lại là không đáng kể.
- Trong những thí nghiệm sử dụng microsome biểu thị CYP hoặc flavin monooxygenase (FM0) của người, cho thấy FM01 và FM03 tham gia tạo chất chuyển hóa chính N-oxide. Tuy nhiên, không phát hiện thấy hoạt tính N-oxygenase của CYP1A2, -2A6, -2B6, -2C8, -2C9, 2C19, 2D6, 2E1, hoặc 3A4.
Đặc điểm
Viên nén tròn bao phim, màu trắng, một mặt trơn, một mặt có mặt ngang chia đôi viên.